“读思达”教学法在高中化学教学中的应用探析
作者: 林云
[摘 要]“读思达”教学法是一种以核心素养为导向的教学方法,它强调学生在学习过程中的主体作用,旨在引导学生通过阅读、思考和表达,发展学生的学科核心素养。将“读思达”教学法运用到“元素周期律”的课堂教学中,通过提问或任务驱动,引导学生自主阅读、积极思考和分享表达,促进学生阅读力、思考力、表达力的发展,从而有效落实化学学科核心素养的培养目标。
[关键词]“读思达”教学法;问题驱动;元素周期律;高中化学
[中图分类号] G633.8 [文献标识码] A [文章编号] 1674-6058(2025)05-0066-04
新课程、新高考、新评价要求着力培养学生的核心素养并促进其个性化发展,这要求在高中化学教学中,教师既要关注基础知识和基本技能的传授,又要关注学生学科能力和学科核心素养的培育。学科知识向学科能力和素养的转化,需经由学生的阅读、思考、表达过程来实现。阅读力、思考力、表达力是学生最基础的学习能力,因此,教师在课堂教学中应提供必要的信息资料,合理创设问题情境,鼓励学生勇于表达个人观点。
在核心素养时代背景下,高中化学教师需积极变革教学方式,依据教学内容选择合适的教学方法进行课堂教学。然而,当前的高中化学教学中存在一些问题,如过度依赖教师讲解,学生阅读兴趣不足,学生自主思考积极性不高,交流讨论及表达观点意愿不强等。为此,教师需要对教学内容进行深入分析,并基于学生的认知发展水平创设问题情境,把问题设置在学生的“最近发展区”,使问题成为学生主动阅读、思考、表达的“引擎”。
一、“读思达”教学法概述
“读思达”教学法是由福建师范大学余文森教授[1]提出的一种教学方法,该方法强调学生在学习过程中的主体地位,通过阅读、思考和表达提高学生的学习能力和学科素养。“读思达”教学法能够充分调动学生学习的积极性和创造性。
“读”即阅读,它涵盖了新课学习前的自主预习,如阅读课本内容(包括目标预览、方法导引、科学史话、学科提炼、拓宽视野等部分),以及查阅文献资料、了解实验步骤、观察实验现象等。此外,新课学习后的习题练习、知识巩固、研究性学习等也属于化学学科“读”的范畴。通过阅读,学生能够初步了解和理解化学概念以及基本的化学原理等。
“思”即思考,是对接收到的信息进行分析、推理、整合、加工的过程。这包括思考科学家所体现的精神、实验现象产生的原因、化学反应的实质以及解决问题的方法等。这些思考活动有助于培养学生的证据推理能力和科学探究意识,进而促进学生创新意识的发展。
“达”即表达,是对知识消化吸收、重构整合之后的输出过程,包括课堂上与同学的交流讨论、回答问题等口头语言表述,还包括对实验现象的描述、化学方程式的书写、原因分析、习题解答、错题整理、反思总结等。阅读、思考、表达是化学学习过程中的三个关键环节,它们相互促进[2]。
接下来,笔者以苏教版高中化学教材必修一专题5第一单元第一课时“元素周期律”的教学为例,阐述如何运用“读思达”教学法进行高中化学课堂教学实践。
二、教学分析
(一)教学内容分析
《普通高中化学课程标准(2017年版2020年修订)》对“元素周期律”的教学提出了如下要求:结合有关数据和实验事实认识原子结构、元素性质呈周期性变化的规律;讨论第三周期元素金属性、非金属性的递变,建构元素周期律;借助元素周期律预测硅、硒、锗、镓等元素的性质,体会元素周期律在学习元素化合物知识与科学研究中的重要作用;查阅元素周期律对发现新元素、制造新物质、开发新材料的指导作用[3]。
“元素周期律”的学习是在原子核外电子排布的基础上,认识元素性质的变化规律,建立观点、结论和证据之间的逻辑关系,并能运用所建构的模型来解释化学现象,揭示现象的本质和规律,旨在培养学生的证据推理与模型建构能力。
(二)教学目标分析
1.通过阅读相关数据和事实,知道原子核外的电子排布、原子半径以及化合价的周期性变化规律,培养“证据推理与模型认知”核心素养。
2.以3~9号、11~17号元素为例,掌握同周期元素的金属性、非金属性变化规律,建构元素周期律,了解科学探究的方法。
3.建构元素周期律的认知模型,能运用模型预测元素的某些性质,体会元素周期律对科学研究的重要意义。
(三)教学思想分析
为了达成以上教学目标,本教学设计注重引导学生从多角度观察与分析数据,使他们能够基于证据认识元素性质的变化规律,通过科学探究建立证据与结论之间的逻辑关系,并学会运用“观察”“实验”“比较”等科学方法;通过小组讨论、反思再探等活动,进一步认识元素性质与原子核外电子排布的关系,经历“数据分析→探寻本质→建立模型→应用模型”的过程,加深对元素性质周期性变化的认识,深刻领悟元素周期律的丰富内涵。
三、教学过程
环节一:情境导入,引出主题
【情境】阅读“门捷列夫的故事”,了解门捷列夫在1867至1871年间研究发现元素周期表的过程:1867年,门捷列夫在编著《化学原理》教科书时,面临一个难题——如何整理当时已知的63种元素,因为当时还鲜有合乎逻辑的组织方式。门捷列夫想到了一个非常巧妙的方法,即利用类似扑克牌的卡片对元素进行分类研究。经过不懈努力,门捷列夫终于在1869年3月归纳出了第一张元素周期表。1871年12月,他在第一张元素周期表的基础上进行改进,发表了第二张元素周期表。第二张元素周期表更加突出了元素性质的周期性,标志着化学元素周期律的发现工作基本完成。
设计意图:通过阅读“门捷列夫的故事”,让学生体会科学家科研过程的漫长与艰辛,明白“只有脚踏实地一步一个脚印,才有可能成功”的道理。借此培养学生勇于探索、坚持不懈的科学精神。
环节二:数据观察,探寻规律
【学生活动1】画出1~18号元素原子的结构示意图,分析1~18号元素的原子最外层电子排布情况,找出规律。
【学生表达1】随着元素原子序数的递增,除氢、氦外,其余元素的原子最外层电子数呈现从1递增到8的周期性变化规律。
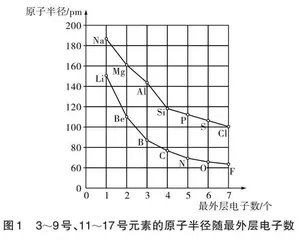
【学生活动2】观察并分析3~9号和11~17号元素的原子半径数据,以元素原子最外层电子数为横坐标,原子半径为纵坐标,在直角坐标系中表示出3~9号、11~17号元素的原子半径随原子最外层电子数变化的曲线。并讨论:随着元素原子序数的递增,元素的原子半径有怎样的变化规律?
【学生表达2】学生自主画图(如图1),总结出:随着原子序数的递增,元素的原子半径呈现周期性变化,3~9号和11~17号元素的原子半径分别依次递减。
【学生活动3】阅读1~18号元素的最高化合价和最低化合价的数据,交流讨论元素化合价的周期性变化,并思考下列问题:
(1)元素的化合价和元素原子序数的变化有什么关系?
(2)元素的最高正价、最低负价和什么因素有关系?最高正价与最低负价之间是否存在关联性?
【学生表达3】当元素的原子序数递增时,其主要化合价也呈现周期性变化。
(1)同周期元素化合价:+1→+7,-4→-1。
(2)元素的最高正价=最外层电子数。
(3)元素的最低负价=最外层电子数-8。
(4)金属元素无负价,氧和氟元素无最高正价。
设计意图:通过展示有关数据和图表,引导学生阅读数据和图表,并经过思考,发现原子核外电子排布、原子半径、元素主要化合价随原子序数递增的变化规律。
【练习巩固】比较下列微粒的半径大小:
Na Na+ O2- F- F- Na+ Cl- Cl Si N
【归纳总结】比较微粒半径大小的依据:(1)微粒半径随着电子层数增多而增大。(2)电子层数相同时,微粒半径随着核电荷数增多而减小。(3)电子层数相同,核电荷数也相同时,微粒半径随着核外电子数增多而增大。
设计意图:在练习中补充离子与原子、离子与离子的半径大小比较,让学生真正理解微粒半径大小的影响因素,从微观角度去理解原子半径的实质。
环节三:深度思考,探索本质
【问题】元素的性质随着原子序数的递增呈周期性变化的根本原因是什么?
【学生】元素的性质与其结构有着密切的联系,主要由元素原子核外电子排布决定。因此,元素性质的周期性变化是原子核外电子排布的周期性变化导致的。
设计意图:通过提问,引导学生进行讨论,深入思考,学会从结构的视角来认识元素性质周期性变化的原因,形成“结构决定性质”的学科观念。
【过渡】当元素原子序数递增时,元素原子的核外电子排布、原子半径和化合价都呈现周期性的变化,那么元素的金属性和非金属性是否也有类似的变化规律?
环节四:科学探究,建立模型
【学生活动4】阅读教材“方法导引”栏目内容,理解元素金属性和非金属性强弱的判断依据。
【问题】如何设计实验,探究钠、镁、铝的金属性强弱?
【学生活动5】小组讨论,设计并实施实验方案。
【归纳总结】学生基于实验结果讨论后得出结论——金属性:Na>Mg>Al。
【问题】如何设计实验,探究硅、磷、硫、氯的非金属性强弱?
【学生活动6】小组讨论,设计并实施实验方案。
【归纳总结】学生基于实验结果讨论后得出结论——非金属性:Cl>S>P>Si。
【建立认知模型】科学猜想→实验设计→实验观察→证据推理。
设计意图:通过阅读文献证据、获取实验证据等,使学生建立证据意识,学会基于证据提出可能的假设,并通过推理加以证实或证伪,建立认知模型,了解证据与结论之间的逻辑关系[4]。
环节五:应用模型,深化理解
表1是元素周期表中的一部分,请参考元素X周边四种元素的性质数据(见表2),预测元素X的最外层电子数、主要化合价、原子半径、元素的金属性或非金属性的强弱。
设计意图:通过运用模型进行科学探究,引导学生深入了解元素的金属性和非金属性的周期性变化规律,初步培养证据推理的能力和严谨求实的科学态度;运用模型推测和解释化学现象,体会元素周期律在科学研究中的重要指导意义。
四、教学效果与反思
(一)教学方法运用得当之处
本节课运用了“读思达”教学法来实施课堂教学,注重化学问题情境的创设,有效激发了学生的学习主动性。在课前预习阶段,学生带着问题开始元素周期律的学习;在课堂上,学生认真阅读,深度思考,积极主动地与同学交流,分组讨论,分工合作,主动分析推理,大胆表达观点,实现了有效的生生互动、师生互动,真正将课堂还给了学生,显著提高了学生的学习效率。该教学方法在其他课例中的应用同样取得了良好效果,形成了良性循环。
(二)需要改进的地方
本校学生程度差别较大,对于后进生,因其基础较薄弱,在阅读时容易走神分心,无法静心学习;在思考讨论时,对一些比较难的问题无法展开思考,碰到问题容易退缩,也不敢表达自己的想法。针对这些现象,教师在设置问题情境时,需要考虑问题设置的层次性,循序渐进,由易到难;在学生分组合作时,可设立小组长,由小组长带头引领,并给组员分配适合的任务。同时,教师要多关注后进生,适时提醒、多提问、多鼓励、多认同,让这类学生也能获得良好的学习体验,学有所得。如此,才能让所有学生实现高效学习,真正提高课堂效率。
综上所述,运用“读思达”教学法进行“元素周期律”的教学是可行且有效的。教师应高度重视学生的阅读,注重问题情境的创设,引导学生深入思考和探究,并鼓励学生进行总结表达,以培养学生的化学学科核心素养,进而促进学生的全面发展。教师在创设问题情境时,需注重问题的启发性、真实性和渐进性,立足教学实际和学情,合理运用生活情境、实验情境、学科史情境等实现学科育人的目标,使学生在解决问题的过程中理解、巩固和运用知识,培养学生的综合素养。
[ 参 考 文 献 ]
[1] 余文森.论阅读、思考、表达的教学意义[J].全球教育展望,2021,50(8):25-43.
[2] 余文森.“读思达”教学法:学生教材学习的基本范式及主要变式[J].中国教育学刊,2021(7):67-72,77.
[3] 中华人民共和国教育部.普通高中化学课程标准:2017年版2020年修订[M].北京:人民教育出版社,2020.
[4] 赵慧存.基于化学学科大概念的单元教学探索与实践[D].漳州:闽南师范大学,2023.
(责任编辑 罗 艳)