氢化物发生原子荧光光谱法测定大米粉中的砷元素
作者: 田翠 徐水莲 杨雪连
摘 要:本文采用氢化物发生原子荧光光谱法测定大米粉中的砷元素。结果表明,砷在0~20.0 ng·mL-1线性关系良好,仪器的检出限为0.18 ng,方法的精密度(RSD,n=7)为1.5%,回收率为93%~106%,测定值与标准值十分接近。
关键词:原子荧光光谱法;砷;大米粉
Determination of Arsenic in Rice Flour by Hydride Generation Atomic Fluorescence Spectroscopy
TIAN Cui, XU Shuilian, YANG Xuelian
(Qingcheng County Food and Drug Testing Center, Qingcheng 745100, China)
Abstract: The determination of arsenic in rice flour by hydride generation atomic fluorescence spectrometry was studied. The results showed that the linear relationship of arsenic was good between 0 ng·mL-1 and 20.0 ng·mL-1, with a detection limit of 0.18 ng for the instrument. The precision of the method (RSD, n=7) was 1.5%, and the recovery rate was 93% ~ 106%. The measured value was very close to the standard value.
Keywords: atomic fluorescence spectrometry; arsenic; rice flour
砷是一种重要的非金属元素,砷及其化合物在自然界分布广泛,对人体有极强的致癌作用,中毒剂量是0.010~0.052 g·kg-1,致死量为0.06~
0.20 g·kg-1[1]。慢性砷中毒会引起皮肤角质化过度、肢体色素沉着、肝脏损伤、神经系统病变等症状,疾病潜伏期为数年甚至数十年,严重时可导致肝硬化、肢体运动障碍、皮肤癌等[2]。其污染物的主要来源是一些冶金企业的非法排污、化工企业的违规排放以及科研场所、学校等实验室的倾倒。被砷污染的土壤和水体可能影响农产品的质量和安全,因此砷作为一种有毒元素已被列为食品安全监督抽检的重点检验项目。食品中总砷的常用测定方法包括电感耦合等离子体质谱法(Inductively Coupled Plasma Mass Spectrometry,ICP-MS)、氢化物发生原子荧光光谱法和银盐法。其中,氢化物发生原子荧光光谱法具有一次性消化样品、操作简便快捷、干扰少、灵敏度高、分析成本低及精密度和准确性好等特点[3]。本实验使用氢化物发生原子荧光光谱法测定大米粉中的总砷含量,确定了样品预处理及仪器测定的最佳条件。
1 材料与方法
1.1 材料与试剂
样品是来自华测检测认证集团股份有限公司的标准物质(BW-21118),特性值为0.647 mg·kg-1,特性值区间为0.543~0.751 mg·kg-1,基质为大米粉;0.5%氢氧化钾溶液;硼氢化钾溶液,10 g·L-1,分析纯;10%硫脲+抗坏血酸溶液,现配现用;5%盐酸溶液;2%硝酸溶液;高氯酸;硫酸;硝酸镁溶液,150 g·L-1,分析纯;氧化镁,分析纯;50%盐酸溶液;水中总砷标准物质,100 mg·L-1(按As计),坛墨质检;砷标准使用液,1.00 mg·L-1,现用现配;实验用水质量符合GB/T 6682—2008一级水规格。除特殊标明外,实验所用试剂均为优级纯。
1.2 仪器与设备
原子荧光光度计:AFS-922,配有计算机处理系统,北京吉天;微波消解仪,MD8H,奥普乐仪器有限公司。
1.3 实验方法
1.3.1 仪器条件
载气:氩气(纯度99.99%);载气流速:
400 mL·min-1;屏蔽气流速:800 mL·min-1;光电倍增管负高压:270 V;灯电流:60 mA;测量方式:荧光强度;读数方式:峰面积;原子化器高度:8 mm;读数延迟时间:1.0 s[4]。
1.3.2 样品预处理
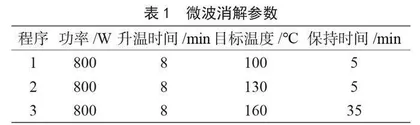
(1)微波消解法。称取0.4 g(精确至0.001 g)样品两份,各加入硝酸7.0 mL,置于赶酸器上120 ℃预消解20 min。旋紧罐盖,按照表1条件进行微波消解,冷却后取出消解罐,慢慢旋转外罐罐盖释放罐内压力,缓慢打开内罐盖子,排放至无黄烟,用少量水冲洗内盖,将内罐置于赶酸器上135 ℃进行赶酸,直至消解液处理至1.0~2.0 mL取出冷却。转移消解液至25 mL比色管中,用少量水洗涤数次,洗涤液合并至比色管中,各加盐酸1.25 mL、10%硫脲+抗坏血酸溶液2.5 mL,补加水至刻度,混匀后45 ℃恒温水浴30 min后测定。同时按同一操作方法做空白实验。
(2)湿法消解法。称取0.4 g(精确至0.001 g)样品两份,置于50 mL三角烧瓶中,加入硝酸
20 mL、高氯酸4 mL、硫酸1.25 mL,过夜后放在电热板上加热消化,温度呈梯度上升,不易过高,使瓶内液体保持微沸状态(消化过程中如果消化液变为棕褐色,则需要取下放冷后补加5~10 mL硝酸)。首先110 ℃加热至消化液澄清,升温至160 ℃进行消化,直至高氯酸的白烟消散,再升温到240 ℃消化,直至硫酸的白烟开始冒出,取出冷却,加入25 mL水,在240 ℃下继续消化,直到出现硫酸的白烟,冷却,将消化液转移到25 mL比色管中,用少量水洗涤三角烧瓶数次,将洗涤液合并到比色管内,加入盐酸1.25 mL、10%硫脲+抗坏血酸2.5 mL,用水定容至刻度,混匀后45 ℃恒温水浴30 min后测定。按同一操作方法做空白实验[5]。
(3)干法消解法。称取0.4 g(精确至0.001 g)样品两份,置于50 mL瓷坩埚中。加入10 mL 150 g·L-1的硝酸镁溶液,混匀,低热蒸干(需蒸干彻底,蒸干终点为样品全部呈焦黄色,否则在炭化时会鼓包,产生的气体会将表面覆盖的氧化镁吹出去,造成损失而影响结果),将1 g(精确至0.001 g)氧化镁尽可能均匀地覆盖在干渣上,于电热板上炭化至无黑烟后,移入马弗炉550 ℃灰化4 h,灰化结束后待马弗炉炉温降低后再打开,取出放冷,缓慢加入10 mL 50%的盐酸溶液,中和氧化镁并溶解灰分,将内溶物转移至25 mL比色管中,加入盐酸1.25 mL、10%硫脲+抗坏血酸溶液2.5 mL,另用水分次洗涤坩埚后合并洗涤液至25 mL刻度,混匀,45 ℃水浴30 min,待测。按同一操作方法做空白实验[6]。
1.3.3 标准曲线的绘制
吸取0.50 mL 1.00 mg·L-1的砷标准使用液于
25 mL容量瓶中,加入盐酸1.25 mL、10%硫脲+抗坏血酸溶液2.5 mL,补加水至刻度,混匀后45 ℃恒温水浴30 min后,仪器设置自动稀释(砷浓度依次为0 ng·mL-1、1.0 ng·mL-1、5.0 ng·mL-1、10.0 ng·mL-1和20.0 ng·mL-1)进行原子荧光强度的测定,绘制标准曲线。
2 结果与分析
2.1 预处理方法比较
不同样品预处理方法测定结果见表2。3种消解方法的实验结果都在允差范围内
[(0.647±0.104)mg·kg-1],湿法消解法实验结果偏高,干法消解法实验结果偏低,微波消解法实验结果十分接近标值。湿法消解法实验过程比较复杂,从安全方面考虑,高氯酸易爆,需严格控制消解温度、赶酸温度、添加消解液的时机,并要防止样品损失;干法消解法耗时较长,样品易损失,氧化镁的含砷量关系到空白值的高低,如果试剂本底值高,空白值就会偏高,从而影响到最终测定结果的准确度。相对而言,微波消解法实验过程更容易操作控制,实验结果更加满意。
2.2 硼氢化钾浓度的选择
硼氢化钾是氢化反应的还原剂,其浓度对荧光信号强度、测定的准确度和稳定性有重要影响。硼氢化钾浓度过低时,还原能力差,气态物难以形成,荧光信号强度弱;硼氢化钾浓度过高时,会有大量氢气产生,稀释样品,引起干扰[7]。因此,要选择合适浓度的硼氢化钾溶液。将浓度为10.0 ng·mL-1砷标准溶液在0.5%、1.0%、2.0%和3.0%的硼氢化钾浓度下分别进行测定,结果见表3。当硼氢化钾浓度为1.0%时砷测定值最接近真实浓度,因此本文还原剂选用1.0%硼氢化钾。
2.3 酸的用量
用国药集团化学试剂有限公司提供的硝酸消解样品,加入7.0 mL硝酸即可将样品消解完全,继续增大硝酸用量时砷测定值变化不大,故本实验选用
7.0 mL硝酸消解样品[8]。
2.4 反应介质与酸浓度的选择
以盐酸、硝酸及高氯酸为反应介质,分别观察其对测定结果的影响。以盐酸为反应介质时灵敏度最高,当酸度在5%~10%时,荧光信号较为稳定。考虑到降低试剂空白和减少酸用量等因素,本实验选择浓度较低的盐酸(5%盐酸)作为反应介质。硝酸和高氯酸具有强氧化性,不适合用于测定砷元素,是因为只有三价砷才能和新生态氢生成砷化氢气体,而硝酸和高氯酸易将三价砷氧化成五价砷。
2.5 线性方程与检出限
调整仪器参数至最佳工作状态,以1%硼氢化钾溶液作还原剂,5%的盐酸作载流,测定砷的荧光强度,绘制标准曲线。砷含量在0~20.0 ng·mL-1时荧光值(I)与浓度(C)呈线性关系,回归方程为
I=11.098 2C-4.244 4,相关系数r=0.999 2。对空白溶液原子荧光强度连续测定11次,计算出仪器的检出限为0.18 ng[9]。
2.6 回收率实验
取1份不含砷元素的试样按微波消解法进行预处理,分别加入高、中、低3个浓度的砷标准使用液,每个浓度水平平行测定5次[10],回收率结果见表4。按照GB/T 27404—2008附录F.1技术要求,被测组分的含量在1~100 mg·L-1时,回收率的允许限为90%~110%,本实验回收率为93%~106%,在允许限内。
2.7 精密度实验
对质量浓度为10.0 ng·mL-1的砷标准溶液连续进行7次荧光强度的测定[11],测定值分别为131.38、130.88、127.95、131.53、133.02、133.12和134.19,相对标准偏差为1.5%。
2.8 准确度实验
取2份质控样(1号质控样来自华测检测认证集团股份有限公司;2号质控样来自粮科院)按微波消解法预处理后进行测定。由表5结果可知,本方法准确、可靠。
3 结论
本研究使用微波消解法处理样品、氢化物发生原子荧光光谱法测定大米粉中的砷元素,方法具有线性良好、检出限低、重现性好、准确度高、减少样品污染和砷元素损失等优点,而且操作简便快速,检测成本相对较低,适用于大米粉中的砷元素的测定。
参考文献
[1]王明强.食品中砷污染的危害及其防治[J].中国酿造,2008(20):87-88.
[2]张维,齐丽娟,宁钧宇,等.砷的健康危害评估[J].毒理学杂志,2021,35(5):367-372.
[3]常迪,王竹天.食品中砷及砷化合物分析方法研究进展[J].国外医学(卫生学分册),2006,33(2):121-125.
[4]韩宏伟,王永芳,赵馨.氢化物发生-原子荧光光谱法同时测定保健食品中砷、汞的研究[J].中国食品卫生杂志,2000(5):7-11.
[5]谢丽玲.原子荧光光谱法测定食品中砷[J].安徽农业科学,2005,33(6):1077.
[6]魏文东.浅谈氢化物原子荧光分光光度法测砷的若干注意事项[J].河南化工,2011,28(12):54-55.
[7]徐燕.微波消解-氢化物发生原子荧光光度法测定食品中的砷和汞[J].预防医学论坛,2008,14(1):47-48.
[8]王洪彬.氢化物发生-原子荧光光谱法测定面粉中微量砷[C]//第二届全国农业环境科学学术研讨会论文集.昆明:中国农业生态环境保护协会,2007:848-849.
[9]廖朝东,陆建平,胡勇辉,等.微波消解样品-氢化物发生-原子荧光光谱法同时测定米粉中砷、汞[J].理化检验(化学分册),2011,47(7):857-858.
[10]徐凤云.应用氢化物发生-原子荧光光谱法联合测定大米中的砷和汞[J].生命科学仪器,2007,5(10):48-50.
[11]臧娜.原子荧光法对食品中砷和汞含量的检测策略研究[J].化工管理,2016(8):251.