葵花籽油制备共轭亚油酸中共轭条件的研究
作者: 邓泽元
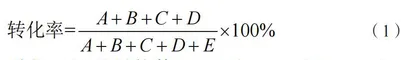
摘 要:葵花籽油混合无水乙醇,通过酶催化得到亚油酸乙酯,以亚油酸乙酯为原料,采用无溶剂碱催化共轭化得到共轭亚油酸乙酯,经皂化酸化得到共轭亚油酸。通过单因素试验得到共轭化过程中最优的反应条件,即反应温度140 ℃,催化剂用量6%,反应时间2 h。并对共轭亚油酸的含量进行检测,在最优条件下共轭亚油酸C18:2(9c,11t和10t,12c)异构体含量达到63.03%,共轭化转化率97.82%。
关键词:葵花籽油;共轭化;共轭亚油酸
Study on Conjugation Conditions of Conjugated Linoleic Acid from Sunflower Oil
DENG Zeyuan
(Heze Zonghoo Jianyuan Biotech Co., Ltd., Heze 274600, China)
Abstract: By mixing sunflower oil with absolute ethanol, ethyl linoleate is obtained by enzyme catalysis. Using ethyl linoleate as raw material, conjugated ethyl linoleate is obtained by solvent-free base catalyzed conjugation, which is acidified by saponification. Conjugated linoleic acid is obtained. The optimal reaction conditions in the conjugation process were obtained by single factor experiment, that is, the reaction temperature was 140 ℃, the catalyst dosage was 6%, and the reaction time was 2 h. The content of conjugated linoleic acid was detected. Under the optimal conditions, the content of conjugated linoleic acid (conjugated linoleic acid C18:2 (9c, 11t and 10t, 12c isomers) reached 63.03%. The conversion rate of conjugation was 97.82%.
Keywords: sunflower oil; conjugation; conjugated linoleic acid
共轭亚油酸(Conjugated Linoleic Acid,CLA)是一类含有顺式和反式共轭双键的十八碳二烯酸异构体的总称。一般认为CLA存在的同分异构体有16种。经过研究发现,CLA主要存在的形式有以下4种:9c,11t-CLA、10t,12c-CLA、9t,11t-CLA、10t,12t-CLA。其中9c,11t-CLA是唯一能被动物细胞吸收进入其磷脂层的异构体,也是与人类和动物营养相关最大、最具有生物活性的CLA[1-3]。CLA具有改善骨质密度、提高机体免疫力、促进脂质氧化分解等生理功能,对癌症、骨质疏松、动脉粥样硬化有一定的抗性作用,还具有减肥降脂的功效[4-5]。
普通植物油中几乎不含CLA,所以如何以较低成本制备出纯度较高的共轭亚油酸成为食品领域研究的焦点[6]。
碱催化异构化法是使用最广泛和最经济的一种制备共轭亚油酸的工业化方法。碱催化异构化法制备共轭亚油酸的原料主要是亚油酸和各种富含亚油酸的天然植物油[7]。葵花籽油又名向日葵油,不饱和脂肪酸丰富,含55%~74%的亚油酸,可成为制备共轭亚油酸的良好材料[8]。本文以高亚油酸含量的葵花油为原料,采用单因素法优化葵花油碱异构化法制备CLA的条件。
共轭亚油酸在紫外区234 nm处有特征吸收峰,而亚油酸却没有。利用这一特征,色谱上常在这个波长下检测CLA的存在和含量,CLA的分析检测方法常用的有紫外检测法和气相色谱法,最佳的是气相色谱法分析测定CLA各种异构体组分[9-12]。
1 材料与方法
1.1 材料
葵花籽油(亚油酸含量65%),来自菏泽中禾健元生物科技有限公司;诺维信脂肪酶435,购自丹麦诺维信公司;强碱催化剂(乙醇钠、乙醇钾等),购自淄博富喜尔化学有限公司;盐酸、无水乙醇、氢氧化钠、无水硫酸钠、氯化钠均为分析纯;三氟化硼甲醇溶液15%、正庚烷、甲醇均为色谱纯。
1.2 仪器
旋转蒸发仪RE-52AA,上海亚荣生化仪器有限公司;电子天平YP6002,余姚市金诺天平仪器有限公司;紫外可见光分光光度计T6新世纪,北京普析通用仪器有限责任公司;真空干燥箱,数显恒温水浴锅HH-4,上海力辰邦西仪器科技有限公司;循环水式多用真空泵SHZ-D(Ⅲ),河南予华仪器有限公司;气相色谱仪A90E,上海仪盟科技有限公司;FID检测器,载气为高纯氮气,燃气氢气,助燃气体空气,色谱柱HP-INNOWAX(30 m×0.25 mm,0.5 μm)。
1.3 实验方法
1.3.1 原料理化性质检验及脂肪酸组成检测
过氧化值的测定参考《食品安全国家标准 食品中过氧化值的测定》(GB 5009.227—2016);酸价的测定参考《食品安全国家标准 食品中酸价的测定》(GB 5009.229—2016);水分及挥发物的测定参考《食品安全国家标准 食品中水分的的测定》(GB 5009.3—2016)。
1.3.2 葵花籽油制备亚油酸乙酯
称取一定量精炼葵花籽油,加入无水乙醇(醇油摩尔比4∶1),加入诺维信脂肪酶435,添加比例占油脂质量的3%~5%,恒温70 ℃搅拌,反应24~36 h。分离过滤脂肪酶,80~90 ℃真空旋蒸脱水脱醇,得到亚油酸乙酯。
1.3.3 亚油酸乙酯共轭化转化生成共轭亚油酸乙酯
将一定量的亚油酸乙酯(要求水分含量低于0.2%)加入到500 mL圆底烧瓶中,打开真空泵(真空度0~500 Pa)加热升温至一定温度,添加一定量的强碱性催化剂,继续真空恒温反应一段时间后,冷却降温至室温,得到共轭亚油酸乙酯。
1.3.4 单因素试验方法
(1)不同反应时间对共轭转化率、CLA含量的影响。称取葵花籽油100 g,选取初始反应温度为140 ℃,加碱量为油脂质量的6%,考察不同反应时间(1 h、2 h、3 h和4 h)对共轭转化率及CLA含量的影响。
(2)不同反应温度对转化率、CLA含量的影响。称取100 g葵花籽油,选取碱添加量为6%,反应时间2 h,考察不同温度(120 ℃、130 ℃、140 ℃、150 ℃和160 ℃)共轭转化率及CLA含量的影响。
(3)不同催化剂用量对转化率、CLA含量的影响。称取100 g葵花籽油,选取140 ℃,反应时间2 h的条件,考察不同催化剂用量(3%、4%、5%、6%和7%)对转化率及CLA含量的影响。
1.3.5 共轭亚油酸乙酯碱醇皂化酸化得到共轭亚油酸
称取原料质量30%的氢氧化钠,并溶解于原料3倍质量的50%乙醇水中,加入到共轭亚油酸乙酯中,于80 ℃恒温搅拌反应4~8 h。用约为皂脚质量10%的稀盐酸(50%体积分数)搅拌酸解,后在70 ℃恒温下静置分液,油层加水反复水洗,直至水层pH值检测为中性结束。取油层于旋转蒸发仪内,85~100 ℃旋蒸脱水,检测水分低于1%。检测样品用无水硫酸钠脱水24 h。
1.3.6 脂肪酸参考质量指标
共轭亚油酸作为新资源食品,其质量指标见表1。共轭转化率、共轭亚油酸的面积百分比计算公式如下:
(1)
共轭亚油酸异构体C18:2(9c,11t和10t,12c)=
A+B(2)
1.3.7 脂肪酸检测条件
脂肪酸组成的测定参考《食品安全国家标准 食品中脂肪酸的测定》(GB 5009.168—2016);氢气流量40 mL/min,空气流量450 mL/min,尾吹气流量(N2)15 mL/min,设定温度210 ℃,保持时间30 min,运行时间30 min,分流比30∶1。脂肪酸前处理方式参考GB 5009.168—2016脂肪的皂化和脂肪酸的甲酯化方法。
2 结果与分析
2.1 葵花籽油、共轭亚油酸脂肪酸检测数据对比
由表2知, 葵花籽油转化共轭亚油酸前后饱和脂肪、不饱和脂肪基本无变化,亚油酸转化为共轭亚油酸,含量大幅下降;共轭亚油酸含量上升。
2.2 反应时间对转化率的影响
由图1可知,随着反应时间的延长,共轭亚油酸转化率和共轭亚油酸含量都呈急速上升趋势,反应时间在2 h时转化率和共轭亚油酸含量处于最大值。但当反应时间超过2 h后转化率呈现下降趋势,共轭亚油酸含量也随之下降,但变化幅度差异不大,综合考虑,选取反应时间2 h。
2.3 催化剂用量对转化率的影响
由图2可知,随着催化剂用量的增加,转化率和共轭亚油酸含量都呈上升趋势,当用量上升到6%时,转化率和共轭亚油酸含量都处于最高值,但当催化剂用量继续上升时,共轭亚油酸含量和转化率反而下降,同时成本也上升。考虑强碱性催化剂遇水分解,大量催化剂快速加入到含水原料中,使得分解反应加快,多余的水分蒸发不及时,反而加速了皂化反应的发生,生成副产物过多,使得催化剂效果变差,影响结果。综上,催化剂选用6%为最优条件。
2.4 温度对转化率的影响
由图3可知,随着温度的升高,共轭亚油酸含量和转化率先是急速上升而后转化率趋于平稳,但共轭亚油酸含量下降。图3中随着温度上升,转化率基本不变,但共轭亚油酸主要异构体含量下降上升,原因可能是温度,全顺式异构体(共轭亚油酸C18:2,9c,12c异构体)和全反式异构体(共轭亚油酸9t,11t和10t,12t异构体)的含量提高,导致共轭亚油酸主要异构体的含量下降。综合考虑,最优反应温度设定为140 ℃。
3 结论
本文初步探讨了葵花籽油制备共轭亚油酸过程中共轭化的条件,葵花籽油混合无水乙醇,通过酶催化得到亚油酸乙酯,以亚油酸乙酯为原料,采用无溶剂碱催化共轭化得到共轭亚油酸乙酯,经皂化酸化得到共轭亚油酸。通过单因素试验得到共轭化过程中最优的反应条件,即反应温度140 ℃,催化剂用量6%,反应时间2 h。在最优条件下共轭亚油酸(共轭亚油酸C18:2,9c,11t和10t,12c异构体)含量达到63.03%,共轭亚油酸C18:2,9c,12c和共轭亚油酸9t,11t和10t,12t含量均符合要求,共轭化转化率97.82%。
参考文献
[1]张绍绍,张慧,李昊昊,等.葵花油碱异构化法制备共轭亚油酸研究[J].中国食品添加剂,2019,30(9):100-105.
[2]刘秋云,李开雄,李宝昆.生物转化共轭亚油酸的研究现状[J].农产品加工(创新版),2010(2):13-16.
[3]冯有胜,丁红梅.共轭亚油酸的结构与性质[J].中国粮油学报,2005(5):97-101.
[4]刘丽娜,缪锦来,郑洲.共轭亚油酸的生理功能综述[J].食品安全质量检测学报,2020,11(8):2552-2557.
[5]李海玲,张思晨,赵志敏,等.共轭亚油酸降脂及分子机理研究进展[J].中国油脂,2022(1):60-67.
[6]郭诤,张根旺,孙彦.共轭亚油酸制备方法的研究进展[J].化学通报,2003(9):592-597.
[7]李琪玲.共轭亚油酸的碱催化异构及其减肥作用研究[D].合肥:合肥工业大学,2012.
[8]毕艳兰.油脂化学[M].北京:化学工业出版社,2005.
[9]陈忠周,李艳梅,赵刚,等.共轭亚油酸的性质及合成[J].中国油脂,2000(5):41-45.
[10]李桂华.共轭亚油酸的制备及其组成分析研究[J].河南工业大学学报(自然科学版),2006(1):7-10.
[11]吴冀华,裘爱泳.气相色谱法分析共轭亚油酸异构体[J].中国油脂,2002(1):65-67.
[12]王伟,杨虹,杨天奎.气相色谱法定量分析共轭亚油酸异构体[J].食品与生物技术学报,2012,31(11):1226-1231.