微波消解-原子荧光法测定牛乳中硒含量的优化实验
作者: 周欢 夏忠悦 钱成林 范光彩 黄漫蓉
摘 要:本文采用微波消解-原子荧光法,通过对比不同的消解参数、赶酸温度、补加盐酸的浓度和体积及后续赶酸时间对检测结果的影响,选择最佳的操作参数,实现对GB 5009.93—2017检测方法的优化,提升可操作性和稳定性。此外,采用优化后的检测方法测定不同地域生牛乳中硒的含量。实验结果表明,试样经微波消解处理后,在150 ℃条件下赶酸50 min,再补加5 mL 6 mol/L的盐酸,继续赶酸15 min,在该处理条件下检测结果相对偏差在2.6%~3.6%,加标回收率在93.04%~97.06%。对不同区域生牛乳中硒含量进行测定,结果表明,山东产地的硒含量最高,达47.94 μg/L,明显高于其他生牛乳。
关键词:硒;生牛乳;原子荧光;参数
Determination of Selenium in Raw Milk from Different Areas by Microwave Digestion Atomic Fluorescence Spectrometry
ZHOU Huan, XIA Zhongyue, QIAN Chenglin, FAN Guangcai, HUANG Manrong
(New Hope Dairy Co., Ltd., Chengdu 610023, China)
Abstract: In this experiment, microwave digestion atomic fluorescence method was used to compare the effects of different digestion parameters, acid driving temperature, hydrochloric acid concentration and volume, and subsequent acid driving time on the detection results, so as to optimize the detection method in GB 5009.93—2017, and improve its operability and stability. In addition, the optimized detection method was used to determine the selenium content in raw milk from different regions. The results showed that the sample was digested by microwave, the acid was removed at 150 ℃ for 50 min, then 5 mL 6 mol/L hydrochloric acid were added for 15 min. Under this condition, the relative deviation of detection results was in the range of 2.6%~3.6%, and the recovery was 93.04%~97.06%. The results showed that the selenium content in Shandong was the highest, up to 47.94 μg/L, significantly higher than other raw milk.
Keywords: selenium; raw milk; atomic fluorescence; parameters
硒具有提高人体免疫力、消除自由基、保护心脏和肝脏等功能,但是我国大部分地区处于低硒带,因此加强对硒的摄入比较重要[1]。研究发现,无机硒(比如亚硒酸钠等)不易被人体吸收,生物有效性低且毒副作用较大,而存在于生物体中的硒(尤其是植物来源的有机硒)是人们摄取硒的主要来源[2-3]。牛奶中含有痕量硒,对牛奶进行硒强化有利于人体吸收。因此,快速准确地测定牛奶中的硒含量具有重大意义。目前测定牛奶中的硒含量可采用湿法消解或微波消解结合原子荧光法、原子吸收光谱法[4],其中微波消解操作简单、快速,被广泛应用于测定食品中的硒含量,但是标准中对赶酸温度与时间等并未进行说明,因此有必要对条件进行优化。本研究用硝酸∶过氧化氢(4∶1)消化样品,对实验条件进行优化,利用氢化物发生-原子荧光光谱法(Hydrid Generation-Atomic Fluorescence Spectrometry,HG-AFS)同时测定了不同产地牛奶中硒的含量,为快速准确测定牛奶中的硒含量提供理论依据。
1 材料与方法
1.1 材料与试剂
生牛乳(四川新华西乳业有限公司);优级纯盐酸(HCl);进口分析纯硝酸(HNO3);优级纯双氧水(H2O2);优级纯铁氰化钾[K3Fe(CN)6];优级纯氢氧化钠(NaOH);优级纯硼氢化钠(NaBH4)。
1.2 仪器与设备
Kylin-S12型原子荧光光度计(北京吉天仪器有限公司);TOPEX+型微波消解仪(上海屹尧仪器科技发展有限公司);赶酸仪(上海屹尧仪器科技发展有限公司);UPR-Ⅱ-20 L型超纯水仪(四川优普超纯科技有限公司)。
1.3 实验方法
1.3.1 标准溶液的配制
(1)硒标准中间液(10 mg/L)。准确量取浓度为1 000 mg/L的硒标准溶液1 mL于100 mL容量瓶中,用5%盐酸定容至刻度,混匀制成10 mg/L的硒标准中间液。
(2)硒标准使用液(1 mg/L)。准确量取浓度为10 mg/L的硒标准中间液10 mL于100 mL容量瓶中,用5%盐酸定容至刻度,混匀制成1 mg/L的硒标准使用液。
(3)硒上机工作液(20 μg/L)。准确量取浓度为1 mg/L的硒标准使用液2 mL于100 mL容量瓶中,加入5 mL铁氰化钾(100 g/L),用5%盐酸定容至刻度,混匀制成20 μg/L的硒上机工作液。
1.3.2 样品前处理
准确称取1.00 g(精确至0.000 1 g)混合均匀的各牛奶样品置于消解罐中加入4 mL硝酸,1 mL双氧水,振摇混合均匀,于微波消解仪中消化,待消解结束,将消解罐放在赶酸仪上继续加热至近干,加5 mL盐酸溶液(6 mol/L),继续加热至溶液变为清亮无色并伴有白烟出现,冷却,转移至25 mL比色管中,加入
2.5 mL铁氰化钾溶液(100 g/L),纯水定容,混匀待测,同时做空白实验[5]。
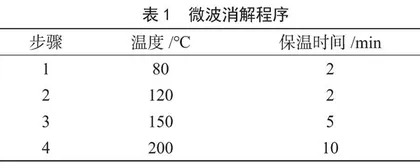
1.3.3 微波消解程序
微波消解程序见表1。
1.3.4 仪器参数
负高压340 V;灯电流100 mA;原子化温度800 ℃;炉高8 mm;载气流速500 mL/min;屏蔽气流速1 000 mL/min;测量方式为标准曲线法;读数方式为峰面积;延迟时间1 s;读数时间15 s;加液时间8 s;进样体积1 mL。
1.3.5 条件优化
(1)通过比对牛奶试样在微波消解时最高温度(200 ℃)的保温时间,验证试样在经过消解后硒的检测回收率。
(2)本实验参考常见的赶酸温度及相关耗材的最高耐受温度,对比选用120 ℃、150 ℃和180 ℃ 3个赶酸温度,同步赶酸30 min,测定硒的加标回收率。
(3)相关文献报道原子荧光检测载流剂浓度差异对检测影响较大,本实验选用5%和10%两组载流剂浓度进行对比实验。
1.3.6 优化后方法的稳定性实验和测试
采用优化后的方法测定2种样品,观察其相对标准偏差和加标回收率,测试该方法的稳定性;采用该方法对不同产地生牛乳的硒含量进行测定,比较各产地生牛乳中硒含量的高低。
2 结果与分析
2.1 消解时间优化
表2为200 ℃下消解不同时间的生牛乳中硒含量的测定结果。由表2可知,随着消解时间的减少,相对标准偏差显著降低(P<0.05),回收率明显增加,为93.04%,这可能是由于硒是热敏性物质,长时间消解会导致硒损失。因此,为确保样品消解完全,本实验确定消解时间为10 min。
2.2 赶酸温度优化
基于硒的热敏性,对赶酸温度进行优化,结果见表3。硝酸分解的中间产物能导致荧光淬灭及荧光强度降低,从而影响测定[6]。消解结束待冷却后,将消解罐放在赶酸仪上加热赶酸至近干,同等条件下150 ℃,50 min能将样液中的硝酸除去,时间较短而且硒浓度值稳定。加入盐酸后再次赶酸,在盐酸介质中,样液中六价硒充分还原成四价硒,四价硒与NaBH4反应生成氢化物,提高盐酸浓度能减少共存元素的干扰并有利于硒元素的还原[7-9]。在用盐酸预还原时,不用蒸太长时间,只要看到有白烟冒出即可停止加热。当赶酸温度控制在150 ℃,13~17 min
时就能看到有白烟冒出,液体略带黄色,但冷却后液体即变成清亮无色,此条件下硒浓度值稳定,加标回收率较高。为实现实验的可操作性和稳定性,最终确定选用150 ℃条件下赶酸15 min。
2.3 载流剂浓度优化
戴瑞平等[10]研究发现,载流剂盐酸浓度影响硒的测定,随着盐酸浓度的增大,荧光强度也随之增大。本实验对5%和10%的盐酸浓度进行比较发现(见表4),其他条件一致,载流剂浓度对回收率无显著性影响(P>0.05),载流剂盐酸浓度为5%时,回收率为96.39%,盐酸浓度为10%时,回收率为97.07%。综合考虑所用盐酸浓度越大对仪器损伤越大的影响。因此,本实验选用浓度为5%的盐酸为载流剂。
2.4 优化后方法的稳定性实验
采用优化后方法测定2种样品。如表5所示,不同样品的相对标准偏差控制在5%以内,加标回收率在93.04%~97.06%,重复性及精确度良好。
2.5 优化后的方法测定不同产地生牛乳的硒含量
由表6可知,采用优化后的方法对不同产地生牛乳的硒含量进行比较发现,山东产地的硒含量最高,达47.94 μg/L,明显高于其他生牛乳。
3 结论
本实验在采用国标方法的基础上对样品微波消解处理后,在150 ℃条件下赶酸50 min,再补加5 mL 6 mol/L的盐酸,继续赶酸15 min,在该处理条件下检测牛奶中硒含量的结果稳定且加标回收率高。采用此参数条件对陕西、四川、山东等地的生乳硒含量进行测定,结果发现除山东高于其他产地外,其余地域生牛乳中硒含量差异不明显。
参考文献
[1]魏增,马怡飞,高文旭,等.盐酸还原氢化物原子荧光法测定牛奶中的硒[J].辽宁化工,2018,47(4):367-368.
[2]丁润梅,田大年.原子吸收法测定市售牛奶中的硒含量[J].石油化工应用,2010,29(6):77-78.
[3]何彩梅,吴桂容,陈春岚,等.食品中硒与硒形态分析方法研究进展[J].食品工业,2017,38(9):218-222.
[4]程建中,杨萍,桂仁意.植物硒形态分析的研究综述[J].浙江农林大学学报,2012,29(2):288-295.
[5]邵奎仲.氢化物-原子吸收光谱法测定牛奶中硒的含量[J].黑龙江科技信息,2008(32):40.
[6]中华人民共和国卫生部.食品安全国家标准 食品中硒的测定:GB 5009.93—2017[S].北京:中国标准出版社,2017.
[7]邓舒美.原子荧光光度法中硝酸酸度的不同对测定硒的影响[J].化工管理,2015(34):193-194.
[8]屈兰竺,常彦彬,石锦铭,等.湿法消解-原子荧光法测定牛奶中的微量硒[J].畜牧与饲料科学,2010,31(1):70-71.
[9]任柯颖.原子荧光光度法测定水质中硒元素[J].科技创新与应用,2020(23):131-132.
[10]戴瑞平,刘花梅,陈林,等.氢化物发生-原子荧光光谱法测定保健品中硒的影响因素[J].化工管理,2019(10):33-35.
基金项目:乳品营养与功能四川省重点实验室(2020YFN0153)。