临床免疫检验的质量控制研究
作者: 崔琳 董丛
摘要:目的 探究对临床免疫检验过程中实行优化质量控制的临床价值。方法 选取我院2021年1月~2022年1月收治的76例参与临床免疫检验的患者作为研究对象,按照检验时间将患者分为对照组(38例)与观察组(38例),对照组采用常规质量管理方法,观察组采用优化质量管理方法。比较两组患者相关变异指数、检验准确率、不良事件发生率、各项临床免疫检验阳性检出率。结果 观察组患者相关变异指数低于对照组(P<0.05);观察组患者检验准确率、临床免疫检验阳性检出率高于对照组(P<0.05);观察组患者不良事件发生率低于对照组(P<0.05)。结论 对临床免疫检验实行优化质量控制,能有效降低临床变异指数,提升检验准确率,提高检验满意度,减少不良事件发生率,提升临床免疫检验阳性检出率。
关键词:临床免疫检验;优质质量控制;检验准确率;检验满意度
临床免疫检验能为患者治疗工作进一步开展提供依据[1]。但临床免疫检验属于较为复杂的过程,受多种因素影响。常见影响检验结果的因素包括检验人员的检验能力、技术掌握情况、环境因素、患者配合程度等[2]。为了提升患者免疫检验效果,减少检验中不良事件的发生,检验科应采取较为有效的检验质量控制方式、优质质量控制方式优化质量,引导检验人员更加关注检验细节,坚持以人为本,保障临床免疫检验准确性[3]。本研究旨在探讨对临床免疫检验过程中实行优化质量控制的临床价值。
1资料与方法
1.1 一般资料
选取我院2021年1月~2022年1月收治的76例参与临床免疫检验的患者作为研究对象,按照检验时间将患者分为对照组(38例)与观察组(38例)。对照组男19例,女19例;年龄28~72岁,平均年龄(45.64±3.44)岁。观察组男20例,女18例;年龄29~73岁,平均年龄(45.48±3.48)岁。两组一般资料比较差异无统计学意义(P>0.05),具有可比性。患者均于我院接受临床免疫检验,对研究与检验工作知情,签署《知情同意书》,各项临床资料完整且清晰可查。
1.2 方法
1.2.1 对照组进行常规质量控制
遵循临床免疫检验流程对该工作进行质量管理,及时处理检验中存在的问题,确保检验工作顺利完成。
1.2.2 观察组优化质量控制
制定完善的临床免疫检验制度,完善标本采集、运输工作。提前了解检验内容,完善检验中所需仪器设备等,遵循无菌性原则。对激素类药物检测的标本,在采集过程中应严格控制标本采集时间,并注重对患者体位的调整。检验前建立完善的档案,对患者年龄、受检项目等予以详细记录,避免采集内容混淆。根据患者检验内容以及标本采集具体特征制定完善且合理的标本保存方式[4~6]。例如:对温度敏感的标本,则应将其存放于冷冻层中;血栓素等标本则应在储存中适量添加抗凝剂。但不同的标本采集及保存方式仅仅能在一定程度上提升标本储存时间。在实际检验中,应尽快将采集完成的标本送往检查,避免标本出现变质,影响检验准确性。检验人员在检验工作开展前,应先对标本完整性予以检查,一旦发现信息缺失或不合格标本,则应拒绝完成检验工作,要求重新采集标本后完成检验工作。
对检验中所需试剂以及仪器等进行严格质量管理。在免疫检验工作期间,所需设备以及试剂较多且复杂,需确保这些设备与检验工作标准一致。同时,在检验中,还应严格按照说明书对试剂以及设备予以操作,并严格遵循无菌性原则,确保检验工作顺利开展。
对检验人员提供专业培训,制定完整的培训与考核制度,对检验人员提出更高的要求。在此过程中明确检验工作人员存在的问题,并及时予以改进,指导检验工作人员遵循以人为本原则,并形成终身学习的理念,提升其自身检验知识以及技能。为患者讲解检验基本流程,要求检验人员互相监督与交流,以保证检验结果准确性与可靠性提升。
检验工作完成后,对检验信息予以反复审核,避免漏诊以及错诊的情况发生。对于检验结果,应做好详细记录,形成专业报告,并为后续免疫检验工作提供详细且客观的参考依据[7]。
1.3 观察指标
比较两组患者相关变异指数、检验准确率、不良事件发生率、各项疾病阳性检出率。(1)相关变异指数:对患者括癌胚抗原、血清胰岛素、甲状腺功能、甲胎球蛋白、糖类抗原199、C肽予以比较。(2)比较两组患者检验准确率以及误诊率。(3)不良事件发生率:比较两组患者标本不合格、送检事件错误以及条形码不合格发生率。(4)各项疾病阳性检出率:观察比较两组患者抗原 - 抗体检验阳性率,包括乙肝表面抗原(hepatitis B surface antigen,HBsAg)、乙肝核心抗原(hepatitis B core antigen,HBcAg)、乙肝表面抗体(hepatitis B surface antibody,HBsAb)、乙肝核心抗体(hepatitis B core antibody,HBcAb)。
1.4 统计学分析
数据处理采用SPSS 25.0统计学软件,计量资料以(±s)表示,采用t检验;计数资料用比率表示,采用χ2检验;P<0.05为差异具有统计学意义。
2结果
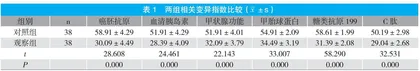
2.1 两组相关变异指数比较
观察组癌胚抗原、血清胰岛素、甲状腺功能、甲胎球蛋白、糖类抗原199、C肽等相关变异指数显著低于对照组(P<0.05)。见表1。
2.2 两组检验准确率比较
观察组检验准确性显著高于对照组(P<0.05)。见表2。
2.3 两组不良事件发生率比较
观察组不良事件发生率显著低于对照组(P<0.05)。见表3。
2.4 两组各项临床免疫检验阳性检出率比较
观察组各项临床免疫检验阳性检出率显著高于对照组,两组阳性检出率比较差异具有统计学意义(P<0.05)。见表5。
3讨论
随着人们生活方式的转变、社会环境的不断恶化,导致多种疾病频发,部分疾病隐匿性较强,对患者身体健康造成较大不良影响的同时导致患者难以发现疾病,延误病情[8]。为此,完善的临床诊断方案对患者产生的影响较大,是后续治疗工作开展的基础性工作,也是影响患者身体健康以及生命安全的重要因素。临床免疫检验是较为常见的临床诊断辅助方式,能判断患者身体免疫能力异常情况,对于鉴别患者疾病发生情况意义显著,能更加直观的反应患者身体内免疫情况,辅助医生了解患者自身免疫状况,进而判断患者疾病发生情况,并予以对症下药。与常规临床生化检验方式比较,临床免疫检验方式较为复杂,流程较为烦琐,且检验结果受外界因素影响较大,对检出率会造成一定影响,不利于后续诊断以及治疗工作开展。故在开展检验工作时,应关注检验质量,对其质量予以细致化控制与管理,尽量减少各种因素对检验结果造成的不良影响。
导致免疫检验结果受到影响的主要因素包括患者因素、标本采集因素、环境因素、设备因素等,多种因素均可能会导致患者标本受到影响,引发不良事件。为此针对影响检验结果的各项因素,应对其实行优质管理干预,加强对于检验全程的质量控制。优质质量管理中,从检验前、检验中以及检验后三个阶段对其进行质量管理。检验前,制定完善的检验制度,可确保检验流程符合检验需求。检验中密切关注各项可能影响检验效果的因素,以确保检验准确性提升。检验后对检验结果进行反复核实,以提升检验结果的可靠性以及准确性。优质质量管理工作开展以及实行,对于避免检验过程中发生检验失误的情况意义显著,同时能为诊疗工作的开展提供可靠的数据支持。
本研究中观察组患者临床相关变异指数较低、检验准确率较高、检验满意度较高、不良事件发生率较低、各项临床免疫检验阳性检出率较高。说明在临床免疫检验过程中,实行优质质量管理,管理效果较佳,可显著改善患者临床检验效果,并能确保检验工作符合临床诊疗效果。其原因与优质质量管理中管理工作人员综合素养较高,具备较为专业的检验方式,并能以较为优质的流程开展检验工作。同时在临床检验过程中,还能不断对检验过程予以调整,及时发现检验过程中可能影响检验结果的问题,并对其予以针对性干预,减少操作中误差情况的发生,并提升临床免疫检验水平。
综上所述,对临床免疫检验中实行优质质量管理方式,能显著降低患者相关变异指数、提升检验准确率、提高检验满意度、减少不良事件发生率、提升各项临床免疫检验阳性检出率,故具有较高临床推广应用价值。
参考文献
[1] 何慧.临床免疫检验质量控制对检验结果可靠性和准确性的影响[J].中国医药指南,2022,20(8):105-107.
[2] 邓涛.对带状疱疹患者实施临床免疫检验质量控制的重要性分析[J].系统医学,2021,6(22):57-59,64.
[3] 马伟刚.溶血标本在应用化学发光免疫分析法检测HIV抗体时对检测结果的影响[J].临床研究,2022,30(9):125-128.
[4] 王钰莹,余丽梅.制备人羊膜间充质干细胞制剂与质量控制过程中关键问题的思考[J].中国组织工程研究,2022,26(25):4016-4021.
[5] 张艳芳,吕虹,邵春青,等.89例自身免疫性脑炎患者临床特征分析[J].国际检验医学杂志,2022,43(6):692-694,700.
[6] 刘冰,王梦莹,肖志良,等.重组人鼠嵌合抗CD20单克隆抗体N糖谱的定性及定量分析[J].中国生物制品学杂志,2022,35(3):289-292.
[7] 王小梅.评估免疫组化染色对临床病理技术质量控制的影响[J].中外女性健康研究,2022(5):187-188.
[8] 张丽艳,元琳.品管圈在临床免疫检验的质量控制应用效果分析[J].健康必读,2022(3):87-88.