液相色谱-质谱联用技术在肉制品中β-受体激动剂类药物残留检测中的应用
作者: 李夸巧,肖植国,罗小珍
摘 要:β-受体激动剂类药物在畜牧业中仍存在非法使用的风险,对消费者健康造成潜在威胁。本文采用液相色谱-质谱联用技术(Liquid Chromatography - Tandem Mass Spectrometry,LC-MS/MS)建立了一种检测猪肉中β-受体激动剂类药物残留的方法。样品经酶解、净化、浓缩后,采用LC-MS/MS在多反应监测(Multiple Reaction Monitoring,MRM)模式下进行定性定量分析。优化后的前处理条件为甲醇-水(70∶30,v/v)作为提取溶剂,37 ℃β-葡萄糖醛酸苷酶水浴酶解12 h,固相萃取净化。优化后的仪器条件为采用C18色谱柱,0.1%甲酸水溶液和乙腈为流动相,梯度洗脱。4种β-受体激动剂在给定浓度范围内与响应值呈良好的线性关系,相关系数均大于0.99;日内和日间相对标准偏差均小于10%,回收率为87.9%~92.5%,基质效应值在90.4%~109.7%。该方法满足肉制品中β-受体激动剂类药物残留检测的要求。
关键词:液相色谱-质谱联用技术;β-受体激动剂;残留;肉制品
Application of Liquid Chromatography - Tandem Mass Spectrometry in the Detection of β-Receptor Agonist Drug Residues in Meat Products
LI Kuaqiao1, XIAO Zhiguo2, LUO Xiaozhen1*
(1.Luoping County Inspection and Testing Institute Yunnan Province, Luoping 655800, China; 2.Qujing Inspection and Testing Research Institute, Qujing 655000, China)
Abstract: β-receptor agonist drugs still pose a risk of illegal use in animal husbandry, posing a potential threat to consumer health. We used liquid chromatography - tandem mass spectrometry (LC-MS/MS) to detect β- receptor agonist drugs in pork. After enzymatic digestion, purification and concentration, the samples were subjected to qualitative and quantitative analysis using LC-MS/MS in multiple reaction monitoring (MRM) mode. The optimized pretreatment conditions were methanol-water (70∶30, v/v) as the extraction solvent, enzymatic hydrolysis of β-glucuronidase water bath at 37 ℃ for 12 h, and solid-phase extraction and purification. The optimized instrument conditions were gradient elution using a C18 column with 0.1% formic acid in water and acetonitrile as mobile phases. The four β-receptor agonists had a good linear relationship with the response value in the given concentration range, and the correlation coefficient was greater than 0.99, the intra-day and inter-day relative standard deviation was less than 10%, the recovery rate was 87.9% to 92.5%, and the matrix effect value was 90.4% to 109.7%. Methodological validation shows that the method meets the requirements for detecting β -receptor agonist drug residues in meat products.
Keywords: liquid chromatography - tandem mass spectrometry technology; β-receptor agonist; residue; meat products
β-受体激动剂是一类高效肉品促生长药物,但β-受体激动剂在动物体内很难被代谢,残留物通过食物链富集,可能危害消费者健康。我国明令禁止在畜禽养殖中使用β-受体激动剂类药物,但养殖户受到经济利益驱动,非法使用时有发生。开发灵敏、准确、快速的检测方法对控制β-受体激动剂类药物非法使用、保障肉制品安全具有重要意义。
1 材料与方法
1.1 仪器与试剂
高效液相色谱仪、三重四极杆串联质谱仪以及配套使用的制水系统。液相色谱采用的色谱柱为C18反相柱。有机溶剂甲醇、乙腈等为色谱纯试剂,水为新鲜制备的超纯水[1]。β-受体激动剂类药物纯度均高于98%。β-葡萄糖醛酸苷酶等辅助试剂选用分析纯级别。样品前处理过程中使用聚合物基质固相萃取小柱净化目标物。
1.2 样品前处理
实验样品选用购自市场的新鲜猪肉,去除脂肪和结缔组织,搅碎均质后置于-20 ℃冷冻保存备用。取2 g肉样于50 mL离心管中,加入10 mL pH值为5.2的醋酸缓冲液,涡旋振荡2 min,超声20 min。加入β-葡萄糖醛酸苷酶,37 ℃水浴过夜,水解样品中的药物结合物,提高游离态药物的提取效率。酶解后样品经C18固相萃取柱净化,甲醇洗脱,氮气吹干后定容,供液相色谱-质谱分析。
为了优化提取条件,本研究考察了甲醇、乙腈、丙酮等常用有机溶剂与水的不同比例(70∶30、50∶50,v/v)混合溶液对β-受体激动剂类药物提取效率的影响。将处理后的肉样分别用不同溶剂组合提取,提取液经净化、浓缩后,采用优化的LC-MS/MS条件进行分析,比较不同提取溶剂组合下目标物的回收率,筛选最佳提取溶剂。
1.3 液相色谱-质谱条件
液相色谱采用Agilent ZORBAX SB-C18色谱柱(100 mm×2.1 mm,1.8 μm),柱温35 ℃。流动相A为0.1%甲酸水溶液,B为0.1%甲酸乙腈溶液,梯度洗脱,洗脱程序如下:0 min 10% B,3 min 50% B,8 min 90% B,10 min 90% B,10.1 min 10% B,12 min 10% B。流速0.3 mL·min-1,进样量为5 μL。质谱采用电喷雾电离正离子模式(ESI+),喷雾电压3 500 V,离子源温度350 ℃,去溶剂气流量1 000 L·h-1,雾化气压力35 psi。
2 结果与分析
2.1 质谱条件优化
2.1.1 母离子和子离子的选择
通过优化质谱条件,选定各目标物的母离子均为[M+H]+准分子离子。母离子经碰撞诱导解离后产生多个子离子,从中挑选出丰度较高、重现性好、受基质干扰小的1个定量离子和1~2个定性离子,构建多反应监测(Multiple Reaction Monitoring,MRM)通道[2]。
2.1.2 碰撞能量的优化
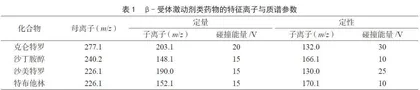
碰撞能量过低,母离子裂解不完全,子离子丰度偏低;碰撞能量过高,子离子过度裂解,灵敏度下降。为获得最佳检测灵敏度,需要优化每个特征离子的碰撞能量。通过调整碰撞能量,考察子离子丰度变化,绘制碰撞能量-离子丰度曲线,选择子离子响应最强时的碰撞能量值作为最佳值。各目标物的定量离子和定性离子经优化后的碰撞能量见表1。
2.1.3 色谱条件的优化
本研究采用反相C18色谱柱,考察了流动相组成、梯度洗脱程序、柱温等因素对分离效果的影响[3]。结果表明,以0.1%甲酸水溶液和乙腈为流动相,梯度洗脱,柱温35 ℃时,各目标物得到良好的分离。优化后的液相色谱条件能在12 min内完成所有待测物的分离分析,色谱峰型对称,基线平稳,无明显拖尾现象,为准确定量提供了良好的基础。
2.2 样品前处理条件优化
2.2.1 提取溶剂的选择
本研究考察了甲醇、乙腈、丙酮等常用有机溶剂和水的不同比例混合溶液对目标物提取效果的影响。由表2可知,甲醇-水(70∶30,v/v)作为提取溶剂时,各目标物的提取效率最高,重复性最好。这可能是因为甲醇-水混合溶剂的极性适中,易于溶解和释放肉样中的极性和非极性药物分子,同时促进了肉样基质的膨胀,有利于目标物的提取。
2.2.2 酶解条件的优化
为准确测定总残留量,需采用β-葡萄糖醛酸苷酶水解样品,释放结合态药物。本研究优化了酶解温度和时间。结果表明,在37 ℃条件下酶解过夜(12 h),药物结合代谢物可完全水解为游离型,酶解效率最高。延长酶解时间至24 h,各目标物的检测量没有明显增加。因此,选择37 ℃水浴酶解12 h作为最佳酶解条件。优化的酶解条件可有效提高β-受体激动剂类药物的检出率,确保检测结果的准确性和可靠性。
2.2.3 净化条件的优化
采用固相萃取(Solid-Phase Extraction,SPE)方式净化样品,考察了不同SPE柱、淋洗液和洗脱液的净化效果。结果显示,使用C18反相SPE柱,以5%甲醇水溶液淋洗,甲醇-水(90∶10,v/v)洗脱,可获得最佳净化效果。与HLB、SCX等其他SPE柱相比,C18柱能更有效地去除肉样基质中的脂肪、蛋白质等杂质,同时减少目标药物的损失。优化的SPE净化条件能最大限度地消除基质干扰,提高检测灵敏度和准确性。
2.3 分析方法的评价
2.3.1 线性范围与相关系数
配制一系列不同浓度(1 μg·kg-1、2 μg·kg-1、5 μg·kg-1、10 μg·kg-1、20 μg·kg-1、50 μg·kg-1、100 μg·kg-1)的药物标准溶液,按建立的样品前处理方法和仪器分析方法测定,以药物浓度为横坐标,响应值(峰面积)为纵坐标,绘制标准曲线,进行线性回归分析[4]。结果显示,4种β-受体激动剂在给定浓度范围内与响应值呈良好的线性关系,相关系数均大于0.99。线性范围覆盖了动物源性食品中β-受体激动剂最大残留限量(Maximum Residue Limit,MRL)的数值,可满足实际样品检测的需求。各药物的线性方程和相关系数见表3。
2.3.2 精密度与准确度
为了评价方法的精密度和准确度,进行了日内和日间重复性试验。精密度通过计算相对标准偏差(Relative Standard Deviation,RSD)来衡量。在3个添加水平(1 μg·kg-1、10 μg·kg-1、100 μg·kg-1)下,每个水平重复6次,连续测定3天,计算日内和日间RSD。准确度采用加标回收率考察。
结果表明,4种β-受体激动剂日内和日间RSD均小于10%,日内RSD为3.5%~4.5%,日间RSD为5.9%~7.2%,表明方法精密度良好。在3个添加水平下,平均回收率为87.9%~92.5%,说明该方法准确度高。