食品中亚硝酸盐检测关键影响因素探究
作者: 王强立
摘 要:目的:运用《食品安全国家标准 食品中亚硝酸盐与硝酸盐的测定》(GB 5009.33—2016)第二法 分光光度法对食品中亚硝酸盐进行检测,分析影响检测结果的关键因素。方法:将标准溶液和待测溶液在同等条件下进行测定,扩展标准曲线线性范围,将检测过程分为4个步骤,分别进行加标回收试验,结合氧化还原反应标准电极电势分析影响检测结果的关键因素。结果:亚铁氰化钾溶液久置后可能分解产生Fe3+,Fe3+可氧化亚硝酸根导致检测结果偏低,其他溶液相对稳定。结论:GB 5009.33—2016中分光光度法稳定可靠,亚铁氰化钾溶液的稳定性是影响检测结果的关键因素。
关键词:食品;亚硝酸盐;亚铁氰化钾;分光光度法
Research on Key Influencing Factors of Determination of Nitrite in Foods
WANG Qiangli
(Xiamen Institute for Food and Drug Quality Control, Xiamen 361013, China)
Abstract: Objective: To detect nitrite in food by GB 5009.33—2016 second method spectrophotometry, and analyze the key factors affecting the test results. Method: The standard solution and the solution to be tested were measured under the same conditions, and the linear range of the standard curve was expanded. The detection process was divided into four steps, and the standard recovery test was carried out respectively. Combined with the standard electrode potential of the redox reaction, the key factors affecting the detection results were analyzed. Result: The potassium ferrocyanide solution may decompose to produce Fe3+ after a long time. Fe3+ can oxidize nitrite, resulting in low detection results, and other solutions are relatively stable. Conclusion: The spectrophotometric method in GB 5009.33—2016 is stable and reliable, and the stability of potassium ferrocyanide solution is the key factor affecting the test results.
Keywords: food; nitrite; potassium ferrocyanide; spectrophotometry
亚硝酸盐主要以钠盐和钾盐的形式存在于食品中,食品中的亚硝酸盐主要来源于人工添加和食品本身。亚硝酸盐可用于食物的增色、保色、抗氧化及防腐[1]。食品本身如蔬菜、肉类、水果等均含有硝酸盐,在加工工艺、保存条件、保存时间以及保存温度等[2-3]的影响下可转化为亚硝酸盐[4],特别是腌制食品易发生亚硝酸盐含量超标[3,5]。亚硝酸盐易与人体中的血红蛋白反应,阻碍人体氧的运输,导致组织缺氧[1],且在酸性条件下易与人体中的胺类物质反应生成致癌物[5-6]。人体(成年人)摄入0.2~0.5 g亚硝酸盐就能引起中毒现象,摄入3 g可引起死亡[5]。因此,食品中亚硝酸盐含量直接影响人类的身体健康,准确测定食品中亚硝酸盐的含量成为检验机构的共同目标。《食品安全国家标准 食品中亚硝酸盐与硝酸盐的测定》(GB 5009.33—2016)已经历多次改版,规定的检测方法有离子色谱法和分光光度法,其中分光光度法由于具有快速、简便、成本低等优势被大多数实验室采用[7],并被广泛应用于快速检测[8]。虽然国家标准经历多次改版,但均未对分光光度法的试剂种类、试剂浓度、显色原理以及显色条件进行修改,表明该方法样品提取、分离、显色的原理稳定、方法可靠。
1 材料与方法
1.1 试剂
亚铁氰化钾、乙酸锌、冰乙酸、硼酸钠、对氨基苯磺酸、盐酸萘乙二胺、盐酸等试剂均为分析纯,国药集团化学试剂有限公司;实验用水为《分析实验室用水规格和试验方法》(GB/T 6682—2008)规定的一级水。亚铁氰化钾、乙酸锌、饱和硼砂溶液于密闭透明广口瓶室温存放;对氨基苯磺酸、盐酸萘乙二胺溶液于棕色瓶密闭、避光冷藏。
1.2 仪器
UV-2700 SHIMADZN紫外可见分光光度计,岛津仪器(苏州)有限公司;DK-S26电热恒温水浴锅,上海精宏实验设备有限公司。
1.3 实验方法
1.3.1 样品制备
参照GB 5009.33—2016第二法 分光光度法,称取一定量肉松、肉松盲样、奶粉质控样[亚硝酸盐含量为(18.0±1.6)mg·kg-1(以亚硝酸钠计)],加入饱和硼砂进行热提取,随后加入亚铁氰化钾溶液和乙酸锌溶液沉淀蛋白质,滤纸过滤,取滤液待测。
1.3.2 系列标准溶液配制
适当扩展标准曲线线性范围[6]。亚硝酸盐系列标准溶液(以亚硝酸钠计):准确移取一定量的亚硝酸盐标准使用液,用纯水稀释定容,得到浓度分别为0.042 µg·mL-1、0.105 µg·mL-1、0.21 µg·mL-1、0.42 µg·mL-1和0.84 µg·mL-1的亚硝酸盐系列标准溶液。
1.3.3 检测方法
参照GB 5009.33—2016第二法 分光光度法,分别移取50 mL的标准溶液和待测液,用对氨基苯磺酸、盐酸萘乙二胺溶液进行显色测定,于538 nm处测定吸光度。本文中的加标浓度和检测结果均表示样品经1.3.1处理后待测液的浓度,盲样、质控样的检测结果为样品实际含量,ND值为未检出,纯水样品均未检出。
2 结果与分析
2.1 标准曲线绘制和扩展
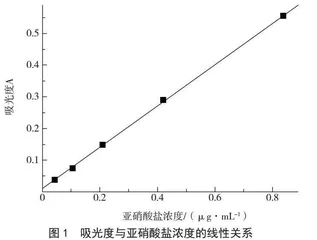
GB 5009.33—2016第二法 分光光度法的标准曲线最高浓度点吸光度较低,仅适用于低浓度样品,对于高浓度样品,需要稀释后重新测定。已有相关文献报道[6],可根据样品需要,适当扩展标准曲线的线性范围,使吸光度在0.2~0.8,甚至更宽,以减少高浓度样品的重复测定,提高检测准确性和检测效率。考虑重氮化反应为放热反应[9],将分光光度法标准溶液的先显色、后定容方式,改进为先稀释定容、再加入显色试剂,将标准溶液与待测溶液在同等条件下测定。按1.3.2绘制标准曲线,如图1所示,以亚硝酸盐浓度为横坐标,吸光度值为纵坐标进行线性拟合,得到线性方程Y=0.649 99X+0.010 59,曲线斜率为0.649 99,截距为0.010 59,相关系数为0.999 82,标准曲线满足测定要求。
2.2 加标回收试验
GB 5009.33—2016第二法 分光光度法未对饱和硼砂、亚铁氰化钾、乙酸锌溶液的保存条件和有效期进行明确说明,仅提及对氨基苯磺酸和盐酸萘乙二胺溶液需置于棕色瓶中避光保存。在实际检测过程中,会存在溶液配制1周甚至1个月后仍在使用的情况,这需要实验室时刻关注并跟踪溶液的变化情况。测试纯水的加标回收率成为检验溶液是否持续有效的重要手段。用新配制和放置1个月的检测溶液(饱和硼砂、亚铁氰化钾、乙酸锌、对氨基苯磺酸和盐酸萘乙二胺溶液),在纯水中添加0.1 µg·mL-1的亚硝酸盐进行加标回收试验,试验结果如表1所示。由表1可知,采用新配制检测溶液进行加标回收试验,加标浓度为0.1 µg·mL-1时,回收率达到98.8%,与相关文献报道相近[10];采用放置1个月的检测溶液进行加标回收试验,回收率仅为47.1%,将蛋白质沉淀时间缩短为10 min,加标回收率提高至75.4%,推测蛋白质沉淀时间会对检测结果产生影响。
进一步将检测溶液放置6个月,在纯水中添加不同浓度的亚硝酸盐进行加标回收试验;在肉松中添加0.25 µg·mL-1的亚硝酸盐进行加标回收试验,放置不同时间后测定回收率,结果如表2所示。对比表1,纯水的加标浓度为0.25 µg·mL-1时,加标回收率由低溶度(0.1 µg·mL-1)的47.1%提高到80.8%;加标浓度为0.75 µg·mL-1时,加标回收率提高到87.3%。肉松加标后直接测定得到的回收率为81.6%;肉松加标后放置1 d再进行测定,加标回收率上升至90.4%;放置2 d后,加标回收率下降至70.4%。结果表明,低浓度样品受检测试剂溶液影响较大。肉松加标回收率受放置天数的影响,表明亚硝酸盐在肉松样品中存在一定的转化[4]。
2.3 各检测步骤对检测结果的影响
将检测过程分为4个步骤:饱和硼砂溶液热提取15 min、亚铁氰化钾溶液和乙酸锌溶液沉淀蛋白质30 min、滤纸过滤样品以及显色。以纯水为样品,通过加标回收试验的方法,考察各检测步骤对检测结果的影响,包括在样品中加标、热提取15 min冷却后加标、蛋白质沉淀30 min后加标以及过滤后加标。仍使用放置6个月的检测溶液进行检测,检测结果如表3所示。由表3可知,热提取15 min冷却后的加标回收率为78.0%,蛋白质沉淀30 min后加标和过滤后加标的回收率分别为99.6%、98.4%,证明滤纸并未吸附亚硝酸盐,且显色试剂稳定有效。结合2.2,缩短沉淀时间、提高加标浓度均可提高加标回收率,推测沉淀剂为影响加标回收率的主要因素。鉴于乙酸锌的化学稳定性,推测加标回收率受亚铁氰化钾溶液影响较大。因此,后续仅重新配制亚铁氰化钾溶液,继续考察加标回收率情况。
2.4 亚铁氰化钾溶液对检测结果的影响
重新配制亚铁氰化钾溶液,其他检测溶液仍使用放置6个月后的溶液,考察纯水和肉松的加标回收率,结果如表4所示。由表4可知,纯水加标浓度为0.25 µg·mL-1时,加标回收率为101.6%,加标浓度为0.75 µg·mL-1时,加标回收率为98.9%;肉松加标浓度为0.25 µg·mL-1时,加标回收率为96.4%,加标浓度为0.75 µg·mL-1时,加标回收率为97.6%。且表5中奶粉质控样(4 g)的检测结果为17.6 mg·kg-1,在质控范围之内,结果准确;肉松盲样检测结果为32.0 mg·kg-1,初滤液为31.8 mg·kg-1,将肉松盲样沉淀后过滤,滤液放置1 d后的检测结果为32.0 mg·kg-1,滤液放置4 d后的检测结果为32.6 mg·kg-1,结果并无太大差异,表明分离沉淀后的滤液稳定,新配制的亚铁氰化钾溶液稳定有效、沉淀过程对亚硝酸盐无影响。增加质控样的称样量时,发现样品提取过程存在结块现象,检测结果为14.3 mg·kg-1,偏离质控范围,且相对偏差较大。
3 讨论
相关文献报道[11],亚铁氰化钾能够与Fe3+生产深蓝色普鲁士蓝,普鲁士蓝水溶性较弱,实验发现长期存放亚铁氰化钾溶液的器壁存在蓝色沉淀,推测久置亚铁氰化钾溶液中存在Fe3+,Fe3+为高价态,具有一定的氧化性,可氧化亚硝酸盐,导致检测结果偏低。2.2中缩短沉淀时间(表1)即减少氧化反应时间、提高加标浓度(表2),2.4中使用新配制的亚铁氰化钾溶液(表4)均能提高加标回收率,进一步证实久置亚铁氰化钾溶液中存在Fe3+。对比氧化还原电位,碱性条件下,NO3-还原成NO2-的标准电极电势为0.01 V[12],Fe3+还原成Fe2+的标准电极电势为0.771 V[13],在久置亚铁氰化钾溶液中可能存在Fe(CN)63-和Fe(CN)64-,Fe(CN)63-还原成Fe(CN)64-的标准电极电势为0.360 V[13]。三价铁两种形态的氧化电位均高于亚硝酸盐,因此,久置的亚铁氰化钾试剂可氧化亚硝酸盐。