六堡茶中茶多糖的含量测定分析
作者: 吴巧妮 潘敏清 何姗珊 李君 陈婵
1.前言
黑茶属于后发酵茶,是中国六大茶之一,主要分为湖南黑茶、广西六堡茶、安徽古黟安茶、云南普洱茶等。其中,六堡茶的产制历史可追溯到1500多年前,其以汤色红浓透亮,香气陈醇,滋味醇厚回甘闻名,也是国家地理标志产品之一。
茶多糖作为一种功效性成分,其为酸性多糖,主要成分有葡萄糖、木糖、阿拉伯糖、甘露糖、半乳糖等,研究发现其具有降血糖、抗氧化、降血脂、增强免疫力等功效。而研究表明,黑茶的茶多糖远远高于红茶和绿茶,其在后发酵期间茶多糖的含量会有所增加,因此,对六堡茶中茶多糖的含量进行分析研究具有深远意义。
邱思绮等人的研究明确了六堡茶多糖中含有中性糖和糖醛酸蛋白质和多酚,但由于茶多糖在提取过程中受颜色的影响较大,因此,目前多用苯酚-硫酸法测定六堡茶的茶多糖,多用蒽酮-硫酸法测定乌龙茶、绿茶等的茶多糖。本试验主要对苯酚-硫酸法和蒽酮-硫酸法测定六堡茶茶多糖的最大吸收波长、曲线线性、样品茶多糖含量、2h内吸光度稳定性、加标回收率和精密度等方面进行研究分析。
2.材料与方法
2.1材料与仪器
试验材料:六堡茶,购自梧州市天誉茶业、广西梧州茶厂、广西梧州茂圣茶厂等。
试验仪器:紫外可见分光光度计(X-7),购自上海元析仪器有限公司;电子天平(Quintix224-1 CN),购自赛多利斯科学仪器(北京)有限公司;数显恒温水浴锅(HH-S8),购自金坛市精达仪器制造有限公司;高性能通用台式离心机(AllegraX-15R),购自美国贝克曼公司。
试验试剂:无水葡萄糖(AR),购自天津市大茂化学试剂厂;蒽酮(AR)、无水乙醇(AR)、丙酮(AR)、正丁醇(AR),购自成都市科隆化学品有限公司;乙醚(AR)、三氯甲烷(AR),购自西陇科学;苯酚(AR),购自麦克林;浓硫酸(GR),购自西陇科学。
2.2溶液配制
0.1mg/mL葡萄糖标准溶液配制:先将无水葡萄糖在105℃干燥箱干燥,恒重后精密称取100mg,用水溶解并定容至1000mL。
5%苯酚溶液配制:称取5g苯酚,溶于100mL水中。
0.2%蒽酮溶液配制:称取0.4g蒽酮,溶于200mL浓硫酸中现配现用。
2.3方法
2.3.1茶多糖提取方法
准确称取1g经粉碎过筛的茶叶,加入15mL水,在70℃的水浴下提取2h后,过滤,润洗残渣2遍,滤液一并收集后用旋蒸仪浓缩至大约10mL,加入无水乙醇至50mL,沉淀24h后,转移至50mL离心管,在4750r/min离心5min后弃去上清液。将沉淀用水重新进行复溶,并定容至40mL,加入1∶1的Sevag试剂,振摇20min,静置分离。收集上清液后定容至50mL,摇匀后精密移取1mL至10mL容量瓶中,并用水定容至刻度,此为样品茶多糖溶液。
2.3.2标准曲线的配制
2.3.2.1苯酚-硫酸法标准曲线的配制
精密吸取0.00、0.10、0.20、0.40、0.60、0.80、1.00mL0.1mg/mL葡萄糖标准溶液(相当于0.000mg,0.010mg,0.020mg,0.040mg,0.060mg,0.080mg,0.100mg葡萄糖)于7支10mL比色管中,用水定容至1mL,再依次加入1mL5%苯酚溶液及5mL浓硫酸,每个试剂加入后都应充分混匀。用涡流均匀器混匀后放置5min后,置于100℃水浴下加热15min,取出放冷。以0管为参比,以葡萄糖含量(mg)为横坐标,以吸光度为纵坐标绘制标准曲线。
2.3.2.2蒽酮-硫酸法标准曲线的配制
精密吸取0.00、0.10、0.20、0.40、0.60、0.80、1.00mL0.1mg/mL葡萄糖标准溶液(相当于0.000mg,0.010mg,0.020mg,0.040mg,0.060mg,0.080mg,0.100mg葡萄糖)于7支10mL比色管中,用水定容至1mL,分别加入0.2%蒽酮溶液3mL,摇匀后置于100℃水浴下加热10min,取出冷却,以0管为参比,以葡萄糖含量(mg)为横坐标,以吸光度为纵坐标绘制标准曲线。
2.3.3测定波长的确定
2.3.3.1苯酚-硫酸法波长的确定
精密移取0.1mg/mL葡萄糖标准溶液1.0mL及样品茶多糖溶液1.0mL,分别置于10mL比色管中,按2.3.2.1自“用水定容至1mL……”起进行操作,测定。
以试剂空白和样品空白为参比,于400-700nm间进行扫描,取两者最大吸收波长。
2.3.3.2蒽酮-硫酸法波长的确定
精密移取0.1mg/mL葡萄糖标准溶液1.0mL及样品茶多糖溶液1.0mL,分别置于10mL比色管中,按2.3.2.2自“用水定容至1mL……”起进行操作,测定。
以试剂空白和样品空白为参比,于400-700nm间进行扫描,取两者最大吸收波长。
2.3.4样品茶多糖的测定
精密移取样品茶多糖溶液1mL,分别按2.3.2.1、2.3.2.2自“用水定容至1mL……”起进行操作,测定。
2.3.5稳定性实验
精密吸取1mL样品茶多糖储备液,分别按2.3.2.1、2.3.2.2自“用水定容至1mL……”起进行操作,测定。
在2h内每30min对其进行吸光度测定,重复3次,考察其稳定性。
2.3.6加标回收率的测定
精密吸取样品茶多糖储备液0.5mL,准确加入0.4mL葡萄糖标准溶液,分别按2.3.2.1、2.3.2.2自“用水定容至1mL……”起进行操作,测定含量,算出回收率。同时每个样品连续测定5次,用于计算方法精密度。
3.结果与分析
3.1原理
3.1.1苯酚-硫酸法原理
经过处理的试样的糖经提取后,用硫酸对试样的多糖进行脱水,生成糠醛或其衍生物。生成物与芳香族酚类化合物缩合生成黄色物质。
3.1.2蒽酮-硫酸法原理
经过处理的试样的糖经提取后,用硫酸对试样的多糖进行水解,脱水成为葡萄糖,在加热和酸性条件下与蒽酮结合成蓝绿色化合物。
3.2吸收波长的比较及确定
精密移取0.1mg/mL葡萄糖标准溶液1.0mL及样品茶多糖溶液1.0mL,分别按2.3.3.1、2.3.3.2操作,在波长400-700nm区域内进行光谱扫描,观察两者最大吸收峰所在的波长。对扫描结果进行比较可以得出,六堡茶茶多糖在苯酚-硫酸法实验中,葡萄糖标准溶液在485nm有最大吸收峰,而六堡茶的茶多糖样品溶液在482nm处有最大吸收峰,无其他干扰峰的存在,说明该方法以葡萄糖为标准品是可靠的。两者的最大吸收峰的波长基本一致。故本方法采用葡萄糖标准溶液的最大吸收峰的波长485nm作为最大吸收波长。
六堡茶茶多糖在蒽酮-硫酸法实验中,葡萄糖标准溶液在592nm,431nm处有较高的吸收峰,六堡茶茶多糖样品溶液在584nm,429nm波长处出现较高的峰值,但由于干扰峰较多,最后参考现有研究决定选择波长590nm作为最大吸收波长。
两种方法相比较,苯酚-硫酸法峰值明显,且无干扰峰,测定准确性较高。
3.3线性比较
以葡萄糖含量(mg)为横坐标,以吸光度为纵坐标,作线性回归。苯酚-硫酸法测定茶多糖的回归方程为c=0.104*A-0.001,相关系数R=0.999580,蒽酮-硫酸法测定茶多糖的回归方程为C=0.122*A+0.001,相关系数R=0.999266,两种方法在浓度为0.01-0.1mg浓度范围内,线性关系良好。
3.4六堡茶茶多糖含量的比较
将样品茶多糖的测定结果(吸光度)分别代入两种方法的标准曲线,再分别算出其样品茶多糖含量,两法测定六堡茶茶多糖含量的测定数据如表1,两种方法的重复性RSD(%)均小于10%,在允许的误差范围内,这说明两种方法的重复性较好,且有较好的重现性;而苯酚-硫酸法的RSD(%)要较蒽酮-硫酸法小,这说明测定结果该法测定六堡茶的重复性更好。
3.5稳定性的比较
每30min对样液茶多糖进行吸光度测定,持续2h,结果如表2。结果表明,苯酚-硫酸法的稳定性较好,2h内吸光度变化值的RSD为1.1%,较为平稳,而蒽酮-硫酸法稳定性不如苯酚-硫酸法,2h内有明显下降,RSD为8.5%,但在1h内稳定性并没有特别明显的下降。
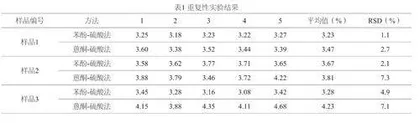
3.6精密度及加标回收率比较
如表3所示,苯酚-硫酸法测定样品平均回收率为100.1%,RSD为1.8%;蒽酮-硫酸法测定样品平均回收率为102.6%,RSD为5.7%;两种方法的加标回收率都符合要求,由表3数据可知苯酚-硫酸法的精密度更好。
结论
本试验用苯酚-硫酸法、蒽酮-硫酸法测定不同六堡茶样品,以葡萄糖作为标准品,分别从两种方法的最大吸收波长、曲线线性、样品茶多糖含量、2h内吸光度稳定性、加标回收率、精密度等方面进行了相关比较,发现两种方法的线性关系良好,重复性、2h内吸光度稳定性、加标回收率、精密度都有较好的表现。但相比较而言,苯酚-硫酸法的最大吸收峰值明显,重复性更好(RSD最高为4.9%),2h内吸光度稳定性更佳(RSD为1.1%),精密度更高(RSD为1.8%)。从样品茶多糖含量的数据来看,蒽酮-硫酸法测得的数据要高一些,虽然苯酚-硫酸法反应剧烈,蒽酮-硫酸法的安全系数会相对更高,但综合所有数据来看,苯酚-硫酸法更适合用于六堡茶茶多糖的测定。