大黄药材HPLC指纹图谱及其真伪鉴别研究
作者: 章平平 甘莉 吴少杰 唐传球
摘要 为了快速有效地辨别大黄,减少大黄的误用,收集了10份来源不同的大黄饮片,从外观形态、显微结构等方面进行研究,同时采用TLC对其进行真伪优劣定性鉴别,并参考《中国药典》2020版一部对大黄的芦荟大黄素、大黄素、大黄酸、大黄酚、大黄素甲醚5个化合物建立了RP-HPLC含量测定。结果表明,10个大黄样品在表面颜色、有无星点及气味强弱等方面均具有一定差异,通过性状鉴别能初略区分真假大黄,但在草酸钙簇晶、导管、淀粉粒、结晶等显微鉴别方面无明显的外观上区别,采用显微鉴别对大黄药材真伪辨别有一定的难度。通过TLC色谱鉴别可以快速有效地分辨出大黄药材的真伪,掌叶大黄和药用大黄均未检出土大黄苷,而华北大黄检出土大黄苷,为伪品。10个大黄样品中游离蒽醌总量均符合2020版《中国药典》限量要求,大黄素甲醚和大黄素含量均较高,其中华北大黄药材中大黄酸含量极少,不到掌叶大黄与药用大黄的含量的1/10。药用大黄和掌叶大黄的指纹图谱相似,与华北大黄具有明显的差异。
关键词 大黄;RP-HPLC;芦荟大黄素;大黄素;大黄酸;大黄酚;大黄素甲醚
中图分类号 R 282.5 文献标识码 A 文章编号 0517-6611(2022)16-0119-04
doi:10.3969/j.issn.0517-6611.2022.16.031
开放科学(资源服务)标识码(OSID):
Study on HPLC Fingerprint of Chinese Rhubarb and Its Authenticity Identification
ZHANG Ping-ping, GAN Li, WU Shao-jie et al
(School of Chemistry and Environmental Engineering, Hanjiang Normal University, Shiyan,Hubei 442000)
Abstract In order to quickly and effectively identify rhubarb and reduce the misuse of rhubarb, 10 pieces of rhubarb from different sources were collected and studied from the aspects of appearance, microstructure, etc. TLC was used to qualitatively identify the authenticity and advantages of rhubarb. With reference to the first volume of Chinese Pharmacopoeia 2020, RP-HPLC was established to determine the content of Aloe emodin,rheum emodin, chrysophanic acid, chrysophanol and emodin ether in rhubarb. The results showed that the 10 rhubarb samples had certain differences in the surface color, whether there were stars and the strength of odor. The true and false rhubarb could be preliminarily distinguished by the character identification, but there was no obvious appearance difference in the microscopic identification of calcium oxalate clusters, ducts, starch granules and crystals. It was difficult to distinguish the authenticity of rhubarb by microscopic identification. The authenticity of rhubarb could be quickly and effectively identified by TLC chromatography. Rhubarb glycoside was not detected in both palmar leaf rhubarb and medicinal rhubarb, while rhubarb glycoside was found in rheum franzenbachii inspection, which was a fake. The total amount of free anthraquinone in the 10 rhubarb samples met the limit requirements of the Chinese Pharmacopoeia 2020. The contents of emodin methyl ether and emodin were relatively high. The content of rhein in rhubarb from rheum franzenbachii was very little, less than 1/10 of that in Rheum palmatum L. and rheum officinale baill. The fingerprints of Rheum palmatum L. and rheum officinale baill are similar, and there are obvious differences between them.
Key words Rhubarb;RP-HPLC;Aloe emodin;Rheum emodin;Chrysophanic acid;Chrysophanol;Emodin monomethyl ether
大黄,在国内和国外都是常用的中药材,它是一种蓼科草本植物,品种很多,是一味临床常用药材,化学成分复杂,主要药效成分为蒽醌类衍生物[1],主要包括大黄酸、大黄素、大黄酚、大黄素甲醚、芦荟大黄素等34种成分[2]。一般将掌叶大黄、药用大黄和唐古特大黄这3个品种称为正品大黄。正品大黄不含土大黄苷,含番泻苷,泻下作用强,而非正品大黄不含番泻苷,只含土大黄苷,无泻下作用或泻下作用很弱;且有资料显示土大黄不含或少含大黄酸[3-5]。
虽然蒽醌类成分并不能作为酸模属土大黄的专属性成分,但2020年版《中国药典》规定大黄含5种游离蒽醌的总量不得少于0.2%[2],而其泻下的主要活性成分番泻苷的含量未作要求,此外,虽然大黄中多成分的含量测定方法均有报道,有薄层色谱法、高效液相色谱-紫外检测法、高效液相色谱-质谱法、高效毛细管电泳法[6-11]。目前,在大黄中各种蒽醌类物质的定量分析中,常采用配备紫外检测器的高效液相色谱仪。相比于比色法、化学光淬灭法和高效毛细管电泳色谱法,高效液相色谱法(HPLC)分离效果好、灵敏度高、重复性好、精确度高,而且设备的价格也比较低廉,在中药的复杂成分分析中广泛的应用。笔者参照中国药典及相关品种质量标准以及相关文献[12-15],以10份来源不同的大黄饮片为研究对象,采用反相高效液相色谱法(RP-HPLC)对不同来源的大黄药材进行研究,建立大黄药材的指纹图谱,为大黄的质量控制提供有效方法。
1 材料与方法
1.1 试验材料
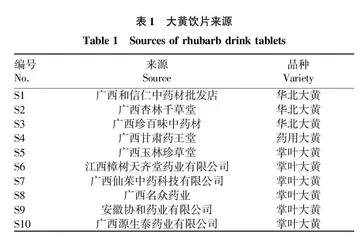
1.1.1 大黄药材。10个样品采购于不同的药店或网上的店铺,采购品种及地点见表1。
1.1.2
主要仪器。显微镜Phemix MC-D500U(C)/TP;ThermoU-3000型高效液相色谱仪(美国,SR-3000 Slvent Rack真空在线脱气机,LPG-3400SDN四元梯度泵,WSP-3000 SLANALYTICAL自动进样仪,Tcc-3000SD柱温箱,VWD-3100二极管阵列检测器)。
1.1.3
主要试剂。芦荟大黄素、大黄素、大黄酸、大黄酚、大黄素甲醚、土大黄苷、大黄对照药材均购自中国食品药品检定研究院;甲醇为色谱纯,购自默克公司。
1.2 试验方法
1.2.1
性状鉴别。通过简单的试验器材进行判别,主要对可见的形状、大小、表面特征、断层面、气味、口感等判别来对药材进行初步鉴别,达到区分中药材的质量和真伪问题。
1.2.2
显微鉴别。以S10为检验样品为例,取饮片粉碎并过4号筛,挑取少量放置在载玻片上,滴加甘油醋酸试液,使得粉末均匀散开,并在酒精灯下微热1 s左右,缓慢盖上盖玻片,放在显微镜下进行观察,观察大黄药材导管、淀粉粒、草酸钙簇晶等内部物质。取少量上述S10粉末,置于蒸发皿上,用滤纸覆盖,采用酒精灯加热,温度不要过高,火焰距离蒸发皿1 cm左右,避免温度过高碳化,加热1 min左右,可以看到有物质附在滤纸上,并进行显微观察。
1.2.3 薄层色谱检查。
1.2.3.1
对照品溶液配制。精密称取土大黄苷0.11 mg于10 mL容量瓶,甲醇定容,超声5 min后,即得。
1.2.3.2
供试品溶液配制。精密称取0.1 g左右大黄细粉(过4号筛),置于锥形瓶中,加甲醇10 mL,超声提取20 min,滤过,精密移取1 mL滤液,用甲醇定容到10 mL容量瓶,摇匀即得。
1.2.3.3
对照药材溶液配制。精密称取0.1 g左右大黄细粉,置于锥形瓶中,加甲醇10 mL,超声提取20 min,滤过,精密移取1 mL滤液,用甲醇定容到10 mL容量瓶,摇匀即得,临用新制。
1.2.3.4
薄层层析。吸取S1~S10供试品溶液、对照药材溶液、土大黄苷对照品溶液各5 L,分别点于同一聚酰胺薄层膜上,以甲苯-甲酸乙酯-丙酮-甲醇-甲酸(30∶5∶5∶20∶0.1)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。
1.2.4 大黄含量测定。
1.2.4.1 对照品溶液的制备。在电子分析天平中分别称取芦荟大黄素对照品1.65 mg、大黄酚对照品1.57 mg、大黄酸对照品0.79 mg、大黄素对照品0.86 mg、大黄素甲醚对照品0.68 mg于5个10 mL容量瓶中,甲醇溶解并用甲醇定容,超声5 min后,得到各对照品溶液。再在5 mL容量瓶内分别加入上述各溶液1~5 mL,配制成对照品混合溶液,其中芦荟大黄素16.219 g/mL、大黄酚15.605 g/mL、大黄酸15.688 g/mL、大黄素16.512 g/mL和大黄素甲醚8.993 g/mL,保存在4 ℃备用。
1.2.4.2
供试品溶液的制备。取本品粉末(过四号筛)0.100 0 g,置于50 mL离心管中,然后精确地加入25 mL甲醇,记录此时的称定重量,用记号笔在离心管液面处画标记线,加热回流1.5 h(在整个过程中,确定该液体是轻微沸腾的),然后将其移出,待温度冷却到在室温下,称其重量。按标志线加适量甲醇,摇晃使其均匀,然后过滤,取出滤液,用0.22 μm的微孔滤膜过滤除去杂质,装入玻璃瓶中,待用。
1.2.4.3
色谱条件。色谱柱为JADE-PAK KM-C 18(250 mm×4.6 mm,5 μm);柱温30 ℃,进样量10 μL;流速1.0 mL/min。二极管阵列检测器(VWD),检测波长280 nm,按照梯度进行洗脱,流动相为甲醇(A)-0.2%磷酸溶液(B),流动相比例(0~10 min,5~30% A;10~40 min,30%~60%A;40~60 min,60%A;60~70 min,60%~100% A;70~75 min,100% A;75~76 min,100%~5% A;76~87 min,5% A)。