电子结肠镜下冷圈套切除术治疗结直肠息肉的疗效与安全性分析
作者: 高清源
摘要:目的 探讨电子结肠镜下冷圈套切除术(CSP)治疗结直肠息肉的疗效与安全性。方法 选取2022年4月~2023年4月医院治疗的400例结直肠息肉患者为研究对象,随机分为对照组和观察组各200例。对照组予以电子结肠镜下高频电凝切除术治疗,观察组予以CSP治疗,比较两组手术指标、息肉完全切除率、复发率、应激指标[去甲肾上腺素(NE)、皮质醇(Cor)]及并发症发生率。结果 两组息肉切除个数比较,差异无统计学意义(P>0.05);观察组手术时间短于对照组,切除次数少于对照组,切口小于对照组(P<0.05);观察组息肉完全切除率高于对照组,息肉复发率低于对照组(P<0.05);观察组术后NE、Cor水平均低于对照组(P<0.05);观察组并发症发生率低于对照组(P<0.05)。
结论 CSP治疗结直肠息肉手术时间短,术中创伤及应激反应轻,息肉完全切除率高,术后复发率及并发症发生率均较低,临床应用效果显著。
关键词:结直肠息肉;电子结肠镜下冷圈套切除术;完全切除率;复发;手术时间
结直肠息肉是发生于结肠和直肠黏膜上的一种良性病变,通常由黏膜增生所致。结直肠息肉在临床中极为常见,通常不会引发相关症状。若息肉较大,患者可能出现腹痛、息肉、便秘、便血等症状,甚至恶变[1]。因此,及早发现、诊断和治疗,对预防结直肠癌具有重要意义。近年来,随着内窥镜技术的不断进步和完善,电子结肠镜下冷圈套切除术(CSP)已逐渐成为治疗结直肠息肉的重要方法。与传统手术干预相比,CSP具有微创、安全、有效等优势,可为患者提供更舒适、有效的治疗[2]。本研究旨在探讨电子结肠镜下冷圈套切除术(CSP)治疗结直肠息肉的疗效和安全性。
1资料与方法
1.1 一般资料
选取2022年4月~2023年4月医院治疗的400例结直肠息肉患者为研究对象,随机分为对照组和观察组各200例。对照组男103例,女97例;年龄23~68岁,平均年龄(52.58±1.34)岁;息肉最大直径4~21 mm,平均直径(9.85±1.43)mm;
单发息肉113例,多发息肉87例。观察组男106例,女94例;年龄为25~70岁,平均年龄(52.72±1.46)岁;息肉最大直径3~20 mm,平均直径(9.43±1.38)mm;单发息肉108例,多发息肉92例。两组一般资料比较,差异无统计学意义(P>0.05)。
纳入标准:经过临床病理检查、结肠镜检查确诊为结直肠息肉;凝血功能正常;存在手术治疗指征。排除标准:疑似息肉癌变;患有其他恶性肿瘤;近1周有抗凝药物使用史;患有严重心脏疾病、脑血管疾病;患有严重器质性疾病。
1.2 方法
1.2.1 对照组给予电子结肠镜下高频电凝切除术
患者取左侧卧位,按流程进行标准消毒、铺巾和麻醉。在结肠镜辅助下,医生确定病变部位和所需切除次数。针对患有多个结肠息肉的患者,从左至右依次切除息肉。结肠镜前端与息肉之间形成适当角度,确保息肉充分暴露,从而便于切除。对于直径<5 mm息肉,用热活检烧灼法进行处理;直径5~20 mm息肉,用高频电圈围绕病灶进行电凝切除;直径>20 mm息肉,先注入氯化钠溶液使病灶部位突出,再用高频电圈套住病灶后进行电凝切除。
1.2.2 观察组给予CSP治疗
完成肠道准备后,将患者体位调整至左侧卧位,静脉麻醉,随后用圈套器经肛门插入内镜,直至回肠末端。在电子内镜引导下,将圈套器送入并轻触肠壁,套取息肉及其基底周边1~3 mm正常黏膜组织,逐渐收紧圈套器,切除息肉。
1.3 观察指标
(1)比较两组手术指标:息肉切除个数、手术时间、切除次数和切口大小。(2)比较两组息肉完全切除率:<6 mm息肉切除率、6~9 mm息肉切除率及>9 mm息肉切除率。(3)比较两组随访12个月的复发率。(4)比较两组应激指标:于术前及术后48 h抽取患者空腹外周静脉血5 mL,以3 500 r/min离心10 min,离心半径为10 cm,获取血清,采用酶联免疫吸附法检测去甲肾上腺素(NE)水平,放射免疫分析法检测皮质醇(Cor)水平。(5)比较两组并发症发生率:如腹痛、肠穿孔、出血等。
1.4 统计学方法
数据处理采用SPSS24.0软件,计量资料以(±s)表示,采用t检验,计数资料以率表示,采用χ2检验,P<0.05为差异具有统计学意义。
2结果
2.1 两组手术指标比较
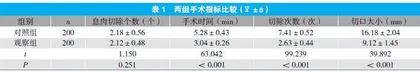
两组息肉切除个数比较,差异无统计学意义(P>0.05);观察组手术时间短于对照组,切除次数少于对照组,切口小于对照组(P<0.05)。见表1。
2.2 两组息肉完全切除率比较
观察组息肉完全切除率为98.50%,高于对照组息肉完全切除率83.50%,两组比较,差异有统计学意义(P<0.05)。见表2。
2.3 两组应激指标比较
术前两组应激指标比较,差异无统计学意义(P>0.05);术后观察组NE、Cor水平均低于对照组(P<0.05)。见表3。
2.4 两组息肉复发率比较
观察组息肉复发率为1.00%,低于对照组息肉复发率5.50%,两组比较,差异有统计学意义(P<0.05)。见表4。
2.5 两组并发症发生率比较
观察组并发症发生率为1.00%,低于对照组并发症发生率5.00%,两组比较,差异有统计学意义(P<0.05)。见表5。
3讨论
结直肠息肉是结肠和直肠黏膜上的常见良性病变,尽管多数为良性,但在一定情况下可能引发一系列临床问题,因此积极治疗结直肠息肉具有重要意义[3]。结直肠息肉,尤其是大型息肉或有恶变迹象的息肉,更容易发展为结直肠癌。早期发现并积极治疗结直肠息肉,可以有效预防癌变[4]。
电子结肠镜辅助下高频电凝切除术是目前广泛应用于结直肠息肉治疗的内镜技术,利用高频电流对息肉进行切除,可以有效清除息肉并能获得较好的病理诊断,利于临床及时发现潜在癌变风险[5]。然而,该技术无法完整切除部分息肉,有一定复发率。CSP为一种新兴的内镜治疗技术,可有效切除各种类型和大小的结直肠息肉,切除率高达90%[6]。相关研究指出,5~20 mm息肉CSP切除成功率和完整切除率均较传统热切除方法更高。CSP操作简单、微创,无需电流直接接触息肉,组织损伤小,出血风险低[7]。本研究结果显示,观察组手术时间短于对照组,切除次数少于对照组,切口小于对照组(P<0.05);观察组并发症发生率、复发率低于对照组(P<0.05)。提示CSP治疗结直肠息肉手术时间短,具有微创性,治疗效果理想、安全性高。CSP是一种相对简单的内镜操作技术,无需复杂的电凝设备和操作步骤,利用冷锋套管直接套住并切除息肉,操作流程短,无需反复切割或灼烧,可大幅度减少手术时间,提高手术效率[8]。CSP冷圈套可完整包围息肉,确保整个息肉组织被彻底切除,避免息肉组织残留及反复切除,降低术后复发的可能性[9]。此外,CSP仅需使用细小的冷锋套管穿过内镜直接切除息肉,切口较小,无需大范围切开[10]。本研究结果显示,观察组NE、Cor水平均低于对照组(P<0.05)。提示CSP治疗结直肠息肉可减轻机体应激反应。CSP手术时间较短,通常15~30 min内即可完成,术中使用冷圈套技术进行切除,可以减少肠道和周围组织的损伤,相比传统手术,创伤程度轻[11~12]。
综上所述,CSP治疗结直肠息肉手术时间短,术中创伤及应激反应轻,息肉完全切除率高,术后复发率及并发症发生率均较低,临床应用效果显著。
参考文献
[1]张丽旻,曾德星.电子结肠镜下冷圈套切除术治疗结直肠息肉患者的临床效果[J].中外医疗,2023,42(29):35-38,43.
[2]阮冠立.电子结肠镜下冷圈套器息肉切除术治疗老年无蒂结直肠息肉患者的效果[J].中国民康医学,2023,35(17):70-73.
[3]王欢.电子结肠镜下冷圈套切除术治疗结直肠息肉的临床疗效及安全性[J].中国医疗器械信息,2023,29(8):70-72.
[4]刘铁柱.电子结肠镜下黏膜切除术对结直肠扁平无蒂息肉患者术后康复及并发症发生率的影响[J].河南医学研究,
2020,29(31):5861-5863.
[5] 戴国栋,高立娟,徐春燕,等.电子结肠镜下冷圈套切除术对较小结直肠扁平无蒂息肉治疗的临床疗效及安全性分析[J].系统医学,2023,8(12):14-17,22
[6]于秀春.电子结肠镜下冷圈套切除术治疗结直肠息肉的临床疗效及安全性[J].中国保健营养,2021,31(2):111.
[7]朱明艳,樊翠翠,颜开华.电子结肠镜下冷圈套切除术治疗对结直肠息肉患者并发症发生率的影响分析[J].世界最新医学信息文摘,2022,22(98):24-27.
[8]李丹丹.电子结肠镜下冷圈套切除术治疗结直肠息肉患者的效果及安全性[J].医疗装备,2021,34(22):84-85.
[9]刘霞,张玲.冷圈套息肉切除术治疗结直肠息肉的研究进展[J].胃肠病学和肝病学杂志,2020,29(8):945-948.
[10]唐林,李朝阳,支娟娟,等.电子结肠镜下冷圈套切除术与高频电凝切除术治疗结直肠小息肉的效果比较[J].临床医学研究与实践,2022,7(6):89-91,108.
[11]王春华,刘伟斌,张海星,等.电子结肠镜下黏膜切除术对于结直肠扁平无蒂息肉治疗的研究[J].中外医学研究,
2019,17(21):110-111.
[12]吴伟,王海浪.电子结肠镜下冷圈套切除术治疗结直肠小息肉的效果[J].安徽医学,2020,41(9):1077-1080.