TP化疗联合曲妥珠单抗治疗HER2阳性乳腺癌的效果观察
作者: 蒙锦莹
摘要:目的 探讨多西他赛+卡铂(TP)化疗联合曲妥珠单抗治疗HER2阳性乳腺癌的临床效果。方法 选取2021年7月~2024年1月于医院确诊为HER2阳性的84例乳腺癌患者为研究对象,随机分为对照组和观察组各42例。对照组给予TP化疗,观察组给予TP化疗联合曲妥珠单抗治疗,比较两组临床疗效、肿瘤标志物水平[癌胚抗原(CEA)、糖蛋白抗原(CA15-3)、组织多肽特异性抗原(TPS)]、生命质量[采用乳腺癌患者生命质量测定量表(FACT-B)]及不良反应发生率。结果 观察组疾病控制率高于对照组(P<0.05);观察组治疗后CEA、CA15-3、TPS水平均低于对照组(P<0.05);观察组治疗后生存质量评分高于对照组(P<0.05);两组恶心呕吐、贫血、肝功能损害、心脏毒性等不良反应发生率比较,差异无统计学意义(P>0.05)。结论 TP化疗联合曲妥珠单抗治疗HER2阳性乳腺癌能够显著提高疾病控制率,下调肿瘤标志物表达水平,改善患者生存质量,且不会明显增加不良反应。
关键词:乳腺癌;HER2阳性;多西他赛;卡铂;曲妥珠单抗
人表皮生长因子受体2(HER2)阳性乳腺癌是一种相对多见的恶性肿瘤,属于乳腺癌的特定亚型,在所有乳腺癌类型中占比高达25%,且近些年的患病率仍不断攀升[1]。化疗是当前临床治疗HER2阳性乳腺癌的常规手段,但化疗药物毒副反应较大,单纯化疗用药效果欠佳[2]。曲妥珠单抗是临床新研制的一种抗肿瘤药物,其对HER2蛋白表达有较为理想的抑制性,用于HER2阳性乳腺癌的治疗效果确切[3]。本研究旨在探讨多西他赛+卡铂(TP)化疗联合曲妥珠单抗治疗HER2阳性乳腺癌的临床效果。
1资料与方法
1.1 一般资料
选取2021年7月~2024年1月于医院确诊为HER2阳性的84例乳腺癌患者为研究对象,均为女性,随机分为对照组和观察组各42例。对照组年龄39~71岁,平均年龄(54.38±7.24)岁;肿瘤分期为Ⅱ期27例,Ⅲ期15例。观察组年龄38~73岁,平均年龄(54.76±7.33)岁;肿瘤分期为Ⅱ期29例,Ⅲ期13例。两组一般资料比较,差异无统计学意义(P>0.05)。本研究已获医院伦理许可。
纳入标准:经临床病理、免疫组织学等综合诊断,确诊为HER2阳性乳腺癌;预计存活期>6个月;
知晓本研究内容并签署知情同意书。排除标准:对研究用药严重不耐受;有精神障碍类疾病;存在严重的肝、肾功能障碍;有严重的系统性疾病,如血液疾病;中途退出或失访。
1.2 方法
1.2.1 对照组给予TP化疗
第1天,静脉滴注多西他赛75 mg/m2,静脉滴注卡铂300 mg/m2,3周为一个化疗周期,持续化疗4个周期。
1.2.2 观察组给予TP化疗联合曲妥珠单抗治疗
TP化疗同对照组;曲妥珠单抗起始静脉滴注剂量为8 mg/kg,之后减少用量至6 mg/kg,每周用药1次,3周为一个化疗周期,持续用药4个周期。
两组治疗期间均给予常规性处理,如保肝、止吐、维持机体水电解质平衡等。
1.3 观察指标
(1)比较两组临床疗效:结合实体瘤评估标准[4]判定。治疗后完全未检出瘤体及新瘤体且持续4周以上,为完全缓解;治疗后瘤体体积减小超过1/2且持续4周以上,为部分缓解;治疗后瘤体体积减小不足1/2或增大不足1/4,为稳定;治疗后瘤体体积增大超过1/4,或出现新瘤体,为进展。疾病控制=完全缓解+部分缓解+稳定。(2)比较两组肿瘤标志物水平:治疗前后抽取患者空腹静脉血3 mL,离心处理10 min后获取血清,检测血清癌胚抗原(CEA)、糖蛋白抗原(CA15-3)、组织多肽特异性抗原(TPS)表达水平。(3)比较两组生存质量:采用乳腺癌患者生命质量测定量表(FACT-B)[5]评估,总分为144分,评分越高表示患者生存质量越高。(4)比较两组不良反应发生率:如恶心呕吐、贫血、肝功能损害、心脏毒性等。
1.4 统计学方法
数据处理采用SPSS24.0统计学软件,计量资料以(±s)表示,采用t检验,计数资料用比率表示,采用χ2检验,P<0.05为差异具有统计学意义。
2结果
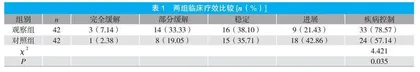
2.1 两组临床疗效比较
观察组疾病控制率高于对照组(P<0.05)。见表1。
2.2 两组肿瘤标志物表达水平比较
两组治疗前肿瘤标志物水平比较,差异无统计学意义(P>0.05);观察组治疗后CEA、CA15-3、TPS水平均低于对照组(P<0.05)。见表2。
2.3 两组生存质量评分比较
两组治疗前生存质量评分比较,差异无统计学意义(P>0.05);观察组治疗后生存质量评分高于对照组(P<0.05)。见表3。
2.4 两组不良反应发生率比较
两组恶心呕吐、贫血、肝功能损害、心脏毒性等不良反应发生率比较,差异无统计学意义(P>0.05)。见表4。
3讨论
相较于其他类型的乳腺癌,HER2阳性乳腺癌通常具有更强的肿瘤增殖活性以及更高的转移率、局部浸润率,临床治疗也较为棘手[6]。TP化疗是现阶段临床用于辅治各类型乳腺癌的常见方案,为全身性作用,在发挥抗肿瘤效果的同时,可不同程度损害机体正常组织细胞,影响治疗效果和患者生存率[7]。因此,临床亟需寻求其他更为有效的方案治疗HER2阳性乳腺癌。
曲妥珠单抗是美国食品药品监督管理局首个获批用于辅治HER2阳性乳腺癌的人源化单克隆抗体,通过与HER2细胞受体特异性结合,阻断HER2与人体表皮生长因子(EGF)发生作用,抑制肿瘤细胞增殖,同时,还可增强免疫细胞、巨噬细胞识别以及攻击肿瘤细胞能力,改善机体免疫力,由此发挥良好的抗肿瘤效果[8]。目前已有多项研究表明,曲妥珠单抗能够让HER2阳性乳腺癌患者在化疗中获益,控制疾病进展,提高患者生存率和生存质量[9~10]。本研究发现,观察组疾病控制率高于对照组(P<0.05);观察组治疗后CEA、CA15-3、TPS水平均低于对照组(P<0.05);观察组治疗后生存质量评分高于对照组(P<0.05)。提示TP化疗联合曲妥珠单抗治疗HER2阳性乳腺癌可获得更为理想的抗肿瘤效果,提高患者生存质量。与李蒙蒙等[11]研究观点基本一致。分析其原因在于,曲妥珠单抗可特异性结合HER2受体,阻断HER2信号通路、诱导肿瘤细胞凋亡、增强免疫系统攻击癌细胞、抑制肿瘤血管生成及细胞周期进程,从而抑制肿瘤细胞的增殖[12]。化疗药物与靶向治疗药物曲妥珠单抗的作用机制不同,二者联用可发挥协同增效作用。两组恶心呕吐、贫血、肝功能损害、心脏毒性等不良反应发生率比较,差异无统计学意义(P>0.05)。说明TP化疗联合曲妥珠单抗治疗不会明显增加患者机体负担。
综上所述,TP化疗联合曲妥珠单抗治疗HER2阳性乳腺癌能够显著提高疾病控制率,下调肿瘤标志物表达水平,改善患者生存质量,且不会明显增加不良反应。
参考文献
[1]郑红梅,吴新红,原俊,等.HER2阳性乳腺癌脑转移3例并文献复习[J].肿瘤防治研究,2015,42(6):637-640.
[2]李岳峰,洪进,李志安,等.HER2阳性乳腺癌接受曲妥珠单抗辅助治疗病人预后分析(附1246例报告)[J].外科理论与实践,2023,28(5):469-476.
[3]刘婷,陈蕾,于力.曲妥珠单抗共轭复合物对HER2阳性乳腺癌疗效及用药安全性的Meta分析[J].中华肿瘤防治杂志,2021,28(17):1345-1354.
[4]梁晓玲,代广全.曲妥珠单抗与帕妥珠单抗联合化疗在HER2阳性乳腺癌患者辅助治疗中的安全性分析[J].中国实用医药,2023,18(17):103-105.
[5]孙岩.多西他赛联合卡铂及曲妥珠单抗新辅助化疗对Ⅰ、Ⅱ期HER2阳性乳腺癌患者的疗效及生存预后的影响[J].中国医学创新,2022,19(12):116-119.
[6]甄洪超,李琴,杜琪,等.曲妥珠单抗辅助治疗对HER2阳性晚期乳腺癌安全性的Meta分析[J]. 临床和实验医学杂志,2020,19(1):43-47.
[7]吴景艳,谢菲菲.曲妥珠单抗联合常规化疗对HER2阳性晚期乳腺癌患者外周血T淋巴细胞亚群及生存率的影响[J].中国合理用药探索,2022,19(10):52-56.
[8]陈佳欣,张会强,周金妹,等.晚期乳腺癌新发脑转移患者继续曲妥珠单抗治疗或更换TKI治疗的疗效和安全性比较[J].解放军医学院学报,2023,44(5):475-480.
[9]朱晓静.曲妥珠单抗联合TP化疗对HER2阳性乳腺癌患者的影响[J].黑龙江医药科学,2020,43(2):133-134.
[10]刘盼盼,马国龙,华燕.曲妥珠单抗联合顺铂治疗HER2阳性乳腺癌患者临床观察[J].内科,2022,17(2):157-159,197.
[11]李蒙蒙,周晓艳.曲妥珠单抗联合TP化疗对HER2阳性乳腺癌的疗效[J].河南医学研究,2021,30(8):1474-1476.
[12]郝凯峰,张明芳,仲广生.吉西他滨联合曲妥珠单抗治疗人表皮生长因子受体2阳性晚期乳腺癌的疗效[J].癌症进展,2023,21(1):105-107.