司美格鲁肽治疗合并肥胖的2型糖尿病患者疗效观察
作者: 马亮【摘要】目的:研究对肥胖症合并2型糖尿病患者使用司美格鲁肽行药物治疗的临床效果。方法:进行回顾性研究,选择我院2022年1月—2022年12月收治的100例肥胖症合并2型糖尿病患者作为研究对象,基于治疗方案对患者进行分组。对照组(50例)采用糖尿病常规治疗方案,观察组(50例)在糖尿病常规治疗方案基础上使用司美格鲁肽,观察两组治疗效果。结果:治疗后,观察组在血糖、BMI等各项指标上优于对照组,差异显著(P<0.05),观察组血压也出现了一定程度的下降。结论:肥胖是诱发2型糖尿病的重要原因。因此,治疗肥胖症合并2型糖尿病,不仅要控制患者的血糖,还要控制患者的BMI。对患者使用司美格鲁肽行药物治疗可取得较好效果。
【关键词】肥胖症合并2型糖尿病;司美格鲁肽;疗效;观察
Observation of efficacy of semaglutide in the treatment of type 2 diabetes patients with obesity
MA Liang
Jiuquan Second People’s Hospital, Jiuquan, Gansu 735000, China
【Abstract】Objective:To study the clinical effect of semaglutide in the treatment of obesity patients with type 2 diabetes.Methods:A retrospective study was conducted,and 100 obese patients with type 2 diabetes admitted to our hospital from January 2022 to December 2022 were selected as the study subjects.The patients were grouped based on the treatment plan.The control group (50 cases) used the routine treatment scheme for diabetes,and the observation group (50 cases) used semaglutide on the basis of the routine treatment scheme for diabetes to observe the treatment effect of the two groups.Results:After treatment,the observation group was better than the control group in various indicators such as blood glucose and BMI,with significant differences (P<0.05),the observation group also showed a certain degree of decrease in blood pressure.Conclusion:Obesity is an important cause of type 2 diabetes.Therefore,the treatment of obesity combined with type 2 diabetes should not only control the blood sugar of patients,but also control the BMI of patients.The use of semaglutide in drug treatment for patients can achieve good results.
【Key Words】Obesity with type 2 diabetes; Semaglutide; Efficacy; Observation
人体摄入的脂肪过多,造成体内脂肪组织堆积过多,导致身体质量指数(BMI)超过正常范围,可诱发肥胖症。世界卫生组织(WHO)已将肥胖症正式确认为一种疾病。肥胖症可引发心血管疾病、高血压、糖尿病、关节炎、呼吸系统疾病等。临床研究表明,许多糖尿病患者明显发胖[1],属于肥胖症合并2型糖尿病。对肥胖症合并2型糖尿病患者开展临床治疗,不仅要控制患者的血糖,还要注意控制患者的BMI、血压、血脂等指标。本次主要研究对肥胖症合并2型糖尿病患者使用司美格鲁肽的治疗效果。
1 资料与方法
1.1资料 进行回顾性研究,选择我院2022年1月—2022年12月收治的100例肥胖症合并2型糖尿病患者作为研究对象,基于治疗方案对患者进行分组。两组基础资料比较无明显差异(P>0.05),具有可比性,详见表1。

1.2 方法
1.2.1对照组 对照组采用糖尿病常规治疗方案。监测患者血糖变化,对患者使用胰岛素等药物治疗。连续治疗12周。
1.2.2观察组 观察组在糖尿病常规治疗方案基础上使用司美格鲁肽。初始阶段持续4周,每周对患者注射1次司美格鲁肽,剂量为0.25mg;维持阶段持续8周,每周对患者注射1次司美格鲁肽,剂量为0.5mg。
1.3 观察指标 本次研究的观察指标,包括:①血糖。采集患者血样,分析血糖指标。②血压。测量患者血压,记录数据,分析血压指标。③BMI。观察、计算患者BMI指数,进行对比。
1.4 数据分析方法 采用SPSS 24.0统计学软件进行数据分析。计数资料采用(%)表示,进行x2检验,计量资料采用(x±s)表示,进行t检验,P<0.05为差异具有统计学意义。
2 结果
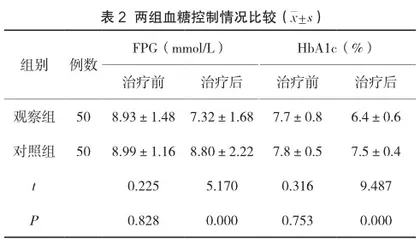
2.1 两组血糖控制情况对比 治疗前,两组血糖指标比较差异不大,P>0.05;治疗后,观察组血糖指标优于对照组,P<0.05,详见表2。
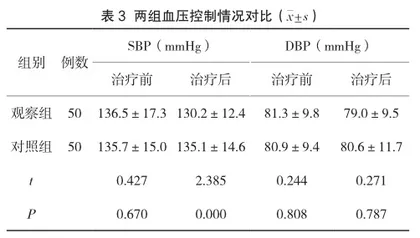
2.2 两组血压控制情况对比 治疗前,两组患者的SBP及DBP比较没有明显差异,P>0.05;治疗后,观察组SBP明显下降(P<0.05),但DBP降幅不明显(P>0.05),详见表3。
2.3 两组BMI情况对比 治疗前,观察组BMI为(31.4±1.3)kg/m2,治疗前,对照组BMI为(31.7±2.3)kg/m2,对比显示t=0.468,P=0.640;12周治疗后,观察组BMI为(26.4±1.1)kg/m2, 12周治疗后,对照组BMI为(31.6±8.9)kg/m2,对比显示t=4.302,P=0.000。治疗前,两组BMI比较差异不大,P>0.05;治疗后,观察组BMI优于对照组,P<0.05。
3 讨论
世界卫生组织(WHO)统计数据显示,超过90%的2型糖尿病患者都有肥胖或超重的问题;在全部2型糖尿病患者中,约有50%的患者患有肥胖症[2-4]。这说明肥胖是造成2型糖尿病发生的主要原因之一。肥胖症本身就是一种慢性代谢性疾病[5-7],肥胖人士体内脂肪细胞过度膨胀,导致脂肪细胞释放大量的脂肪酸。大量脂肪酸会随血流进入肝脏和肌肉细胞,干扰肝脏和肌肉细胞对胰岛素的响应,从而降低胰岛素的效力,导致胰岛素抵抗。肥胖可导致人体内炎症因子的增加,如肿瘤坏死因子(TNF-α)、白细胞介素-6(IL-6)等。肿瘤坏死因子(TNF-α)、白细胞介素-6(IL-6)等炎症因子会干扰胰岛素信号通路,造成胰岛素抵抗。肥胖可导致脂肪细胞激素(如瘦素、肥胖素)的分泌异常。脂肪细胞激素分泌异常会干扰胰岛素的信号传递,从而引起胰岛素抵抗。肥胖可导致细胞膜脂质的改变,使细胞膜上的胰岛素受体数量和活性下降,影响胰岛素的作用。肥胖症合并2型糖尿病导致患者体内发生慢性低级炎症和代谢紊乱(如高胆固醇、高三酰甘油、低密度脂蛋白等代谢异常),进而影响患者多个器官和系统的功能。高胆固醇、高三酰甘油、低密度脂蛋白等代谢异常可导致患者发生心血管疾病,并引起高血压。肥胖症合并2型糖尿病还会影响关节和呼吸系统的健康,增加关节炎和呼吸系统疾病的风险。因此,对于肥胖症合并2型糖尿病的患者,除了控制血糖外,还需要注意控制体重、血压、血脂等代谢指标,降低相关的并发症风险。
人体内存在着长效胰高血糖素样肽-1(Longacting glucagon-like peptide-1,LGLP-1),长效胰高血糖素样肽-1是一种内源性肽类激素,机体每次进餐后,肠道L细胞可分泌出长效胰高血糖素样肽-1。长效胰高血糖素样肽-1可以刺激胰岛素分泌,抑制胰高血糖素分泌,帮助调节血糖水平;长效胰高血糖素样肽-1可以减缓胃肠道排空速度,从而抑制胃排空,减缓食物通过消化道的速度,使饱腹感更强,有助于控制食欲和体重。长效胰高血糖素样肽-1还具有保护胰岛β细胞、抗炎、抗氧化等生物学功能。临床研究表明:在2型糖尿病患者中,由于胰岛素抵抗和胰岛素分泌不足,长效胰高血糖素样肽-1的分泌也会受到影响;造成患者长效胰高血糖素样肽-1水平较低,血糖素样肽-1水平较低又会反过来加重胰岛素抵抗和高血糖。专家们对长效胰高血糖素样肽-1进行分析,发现:人体内的长效胰高血糖素样肽-1半衰期很短,只有几分钟,因此不能作为药物使用。为了解决这一问题,丹麦医学专家提取长效胰高血糖素样肽-1,并对长效胰高血糖素样肽-1进行改良,使其更加稳定和长效。
司美格鲁肽是一种人工合成的肽类药物,其结构高度类似于人体内存在的长效胰高血糖素样肽-1。与长效胰高血糖素样肽-1不同的是,司美格鲁肽的化学结构被改变,半衰期更长(司美格鲁肽的半衰期约为1周左右),因此,司美格鲁肽能够在患者体内长时间发挥作用。司美格鲁肽可以模拟胰高血糖素样肽-1(GLP-1),刺激胰岛素分泌,抑制胰高血糖素分泌,减少胃肠道蠕动,减少胃酸分泌,减缓食物通过胃肠道的速度,增加饱腹感,抑制食欲,从而控制血糖和脂肪摄入量。2017年后,司美格鲁肽在主要发达国家投入临床使用。目前,司美格鲁肽已经被批准在全球范围内用于治疗2型糖尿病,包括美国、欧洲、日本等地。司美格鲁肽可以抑制肾小管对葡萄糖的再吸收,减少钠的重吸收,增加排尿量,并具有一定的血管舒张作用,可以调节血压。
FPG、HbA1c是合并肥胖的2型糖尿病患者临床治疗中的重要观察指标。FPG反映患者的空腹血糖水平,HbA1c是血液中糖化血红蛋白的浓度,它反映了过去2~3个月的平均血糖水平。糖尿病不会直接造成患者死亡,但血糖水平持续升高可造成心血管疾病、神经病变和肾脏疾病等各种并发症,最后导致患者死亡。糖尿病临床治疗始终围绕着控制患者血糖水平这一核心,通过监测和控制FPG水平,可以评估治疗的有效性,并预防并发症的发生。通过监测HbA1c水平,可以评估治疗的长期效果,并调整治疗方案以达到目标血糖水平。合并肥胖的2型糖尿病患者通常会出现明显的胰岛素抵抗,即身体对胰岛素的反应减弱,为了补偿胰岛素抵抗,胰岛会释放更多的胰岛素。然而,胰岛素的过度释放会导致血管收缩,从而增加血压,高血压又会增加心血管疾病的风险,通过监测和控制SBP、DBP水平,可以降低心血管并发症的风险。本次研究结果显示,治疗后,观察组在血糖、BMI等各项指标上优于对照组,差异显著(P<0.05),观察组血压也出现了一定程度的下降,提示司美格鲁肽取得了明显疗效。
综上所述,肥胖是诱发2型糖尿病的重要原因。因此,治疗肥胖症合并2型糖尿病,不仅要控制患者的血糖,还要控制患者的BMI。对患者使用司美格鲁肽行药物治疗可取得较好效果。
参考文献
[1] 张凤丽,张东凤,赵一楠,等.司美格鲁肽对2型糖尿病患者心血管危险因素的影响[J].中国医药, 2022,17(12):1800-1803.
[2] 李宵,丁琮洋,任炳楠,等.国家医保谈判药品新型GLP-1RA司美格鲁肽注射液的数字化遴选评价[J].中国现代应用药学,2022,39(22):2981-2990.
[3] 王文琦,张涛.司美格鲁肽对2型糖尿病合并冠心病患者心肌缺血总负荷及血清炎症因子的影响[J].临床荟萃,2022,37(11):996-1000.
[4] 王海旭,巩秋红.司美格鲁肽口服制剂治疗2型糖尿病的研究进展[J].中国糖尿病杂志,2022,30(11):870-872.
[5] 陈婷,邓斌,廖占林.司美格鲁肽联合二甲双胍治疗初诊2型糖尿病合并非酒精性脂肪肝的疗效分析[J].糖尿病新世界,2022,25(21):81-84.
[6] 孙倩,谭伟.司美格鲁肽治疗肥胖型2型糖尿病的研究进展[J].中国现代医生,2022,60(29):117-120.
[7] 杨曦,何欣瑶,雷相国.司美格鲁肽对非糖尿病超重或肥胖成年人群减重作用的系统评价[J].广西医学,2022,44(19):2285-2291.