两种方法在乳粉中金黄色葡萄球菌(定量)能力验证中的应用
作者: 杨生梅 辛翠霞 高平林 田小琴 吴其其 段爱莉
摘 要:目的:验证本实验室定量检测金黄色葡萄球菌能力,提升检测技术和服务水平。方法:应用国标方法与3M PetrifilmTM金黄色葡萄球菌测试片计数法两种方法进行金黄色葡萄球菌定量检测。结果:国标方法测得乳粉样品(TF04900003)金黄色葡萄球菌的含量为7 900 CFU·g-1,乳粉样品(TF04900004)金黄色葡萄球菌的含量为8 400 CFU·g-1,验证结果为满意。结论:本实验室具备金黄色葡萄球菌定量检测能力。
关键词:金黄色葡萄球菌;能力验证;3M PetrifilmTM金黄色葡萄球菌测试片
Application of Two Methods in Quantitative AbilityVerification of Staphylococcus aureus in Milk Powder
YANG Shengmei, XIN Cuixia, GAO Pinglin, TIAN Xiaoqin, WU Qiqi, DUAN Aili*
(Wuwei City Food Inspection Testing Center, Wuwei 733000, China)
Abstract:Objective: To verify the quantitative detection capability of Staphylococcus aureus in our laboratory and improve the detection technology and service level. Method: Two methods, namely the national standard method and the 3M PetrifilmTM Staphylococcus aureus test strip counting method, were used for quantitative detection of Staphylococcus aureus. Result: The content of Staphylococcus aureus in the milk powder sample (TF04900003) was determined to be 7 900 CFU·g-1 by the national standard method, and the content of Staphylococcus aureus in the milk powder sample (TF04900004) was 8 400 CFU·g-1. The verification results are satisfactory. Conclusion: This laboratory has the ability to quantitatively detect Staphylococcus aureus.
Keywords: Staphylococcus aureus; capability verification; 3M PetrifilmTM Staphylococcus aureus test strip
能力验证是评价实验室技术能力的有效手段,也是实验室进行质量控制的重要环节[1]。金黄色葡萄球菌是革兰氏阳性菌,在自然界广泛分布,能引起严重的化脓性感染和疾病,对人类呼吸道、皮肤、血液及肠道等组织均具有一定的攻击性[2]。金黄色葡萄球菌繁殖过程产生的肠毒素,是引发食物中毒的主要致病因子[3]。国家对食品、药品及化妆品等产品中的金黄色葡萄球菌限量进行明确规定,其中,《化妆品安全技术规范》《中华人民共和国药典》中规定金黄色葡萄球菌不得检出,《食品安全国家标准 预包装食品中致病菌限量》(GB 29921—2021)[4]中规定巴氏杀菌乳、调制乳、发酵乳、加糖炼乳(甜炼乳)和调制加糖炼乳中金黄色葡萄球菌不得检出,乳制品中干酪、再制干酪和干酪制品,肉制品,粮食制品,即食豆制品,即食果蔬制品,冷冻饮品,即食调味品的残留限量允许为采样量5,最多允许有2个值在100~1 000 CFU·g-1(mL-1)。《食品安全国家标准 散装即食食品中致病菌限量》(GB 31607—2021)[5]要求散装即食食品金黄色葡萄球菌≤1 000 CFU·g-1(mL-1)。金黄色葡萄球菌常见的检测方法为国标方法,该方法要先进行传统生物学培养,再进行生化鉴定,其中生化鉴定步骤复杂,检测时间长且易出现假阴性,本文采用国标方法进行检验的同时应用3M PetrifilmTM金黄色葡萄球菌测试片计数辅助判断试验结果,有效确保了实验结果准确性。
1 材料与方法
1.1 材料与仪器
1.1.1 样品来源
NIFDC-PT-490乳粉中金黄色葡萄球菌(定量)检验能力验证共发放2份待测样品,样品编号为TF04900003、TF04900004(实验室内部编号为1、2),每份样品包含1个菌球与1袋奶粉基质,均由中国食品药品检定研究院提供。
1.1.2 标准菌株
阴性对照菌株:大肠埃希氏菌ATCC25922-1;阳性对照菌株:金黄色葡萄球菌ATCC6538-1,两种菌株均为本实验室的储备菌株。
1.1.3 培养基及试剂
无菌生理盐水、Baird-Parker平板(BP平板)、血琼脂平板(血平板)、冻干血浆、脑心浸出液肉汤(BHI肉汤)、营养琼脂小斜面(NA斜面)以及革兰氏染色液,均购自北京陆桥生物技术有限公司;3MPetrifilmTM金黄色葡萄球菌测试片,购自3M公司。
1.1.4 仪器与设备
立式压力蒸汽灭菌器,冰山松洋生物科技(大连)有限公司;无菌均质器,上海比郎仪器制造有限公司;立式智能生化培养箱,上海一恒科学仪器有限公司;生物安全柜,苏州市华宇净化设备有限公司;移液枪,艾本德中国有限公司;生物显微镜,麦克奥迪实业集团有限公司。
1.2 试验方法
1.2.1 样品前处理
在生物安全柜内,取225.0 mL灭菌生理盐水加入无菌均质袋内,将西林瓶内编码为TF04900003小球加入生理盐水中,充分溶解,再将与小球相同编码的奶粉样品25 g加入灭菌生理盐水中,用无菌均质器均质2 min,制成10-1的样品匀液,用移液枪吸取1 mL样品匀液,加入9 mL生理盐水中,制成10-2的样品稀释液,按以上步骤依次制成10-3、10-4、10-5的样品稀释液,TF04900004样品重复上述操作。
1.2.2 样品涂布及培养
将1.2.1中5个稀释度的样品匀液以0.30 mL、0.30 mL、0.40 mL的量分别接种于BP平板上,并用L棒均匀涂布平板,注意样品尽量不要涂布到平板边缘,涂布结束后,正置平板于36 ℃培养箱中,吸收1 h后倒置平板,继续培养48 h。
1.2.3 典型菌落计数与确认
筛选符合金黄色葡萄球菌典型特征的平板,选择同一浓度3个平板典型菌落数之和在20~200 CFU的平板计数,同时进行生化验证。从所选择的平板上挑取至少5个可疑菌落,分别做革兰氏染色镜检、血浆凝固酶试验并接种血平板观察菌落形态,同时以金黄色葡萄球菌ATCC6538-1菌种作为阳性对照,以大肠埃希氏菌ATCC25922-1作为阴性对照。①革兰氏染色镜检。根据试剂盒说明书从每份样品中选取5个可疑菌落进行染色镜检,并在显微镜下观察。②血浆凝固酶试验。将挑取的5个可疑性菌落接种到5 mL脑心浸出液肉汤中,同时接种营养琼脂小斜面,放置于36 ℃培养箱中培养24 h后,取培养物0.3 mL加入0.5 mL冻干血浆中,振荡摇匀后,放置于36 ℃培养箱中培养,6 h内定时观察血浆凝固情况。③血平板。在接种脑心浸出液肉汤和营养琼脂小斜面的同时划线接种血平板,36 ℃培养24 h后观察菌落形态。
1.2.4 3MPetrifilmTM金黄色葡萄球菌测试片计数
将3MPetrifilmTM金黄色葡萄球菌测试片平铺在无菌台面上,揭开表面的膜,分别取5个浓度的稀释液1 mL加入测试片中心,再将表面膜缓缓盖上,用无菌镊子轻轻按压,使样液尽可能均匀分布于圆形培养面,静置,待培养基凝固后将测试片透明面向上放回原自封袋中进行培养,培养条件为36 ℃,24 h左右,每个浓度做2个平行实验,接种无菌生理盐水1 mL作为阴性对照。
2 结果与分析
2.1 BP平板计数
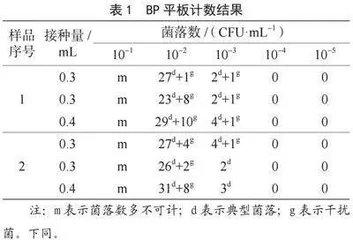
样品1和2在BP平板上有3种形态,一种呈圆形、黑色菌落,表面光滑、凸起、湿润,菌落直径为2~3 mm,有浅色边缘,周围绕以不透明圈,其形态和金黄色葡萄球菌典型菌落形态相符合,标记为典型菌落;一种与典型菌落大小、颜色相似,无浅色边缘,也无不透明圈,与金黄色葡萄球菌典型形态不符合,为干扰菌,排除;另一种有浅色边缘及不透明圈,但较前两种菌直径较小,约为1 mm,不符合金黄色葡萄球菌直径范围,也是干扰菌,排除。经过对有典型菌落的平板进行计数,筛选出适宜计数菌落浓度为10-2,分别计数样品1和2在各个浓度上的菌落数,结果见表1。
2.2 生化鉴定结果
样品1和2各5个可疑菌落经过革兰氏染色后,在100倍镜下均为蓝紫色,呈葡萄球状排列,无荚膜,无芽孢,镜检结果与阳性标准菌株ATCC6538-1一致,为革兰氏阳性菌。将样品1、2各5个可疑菌落脑心浸出液肉汤培养物接种于冻干血浆后每30 min观察1次,均于3 h后开始凝固,4 h后基本凝固,阳性标准菌株ATCC6538-1于2 h后开始,3 h后完全凝固,阴性对照ATCC25922-1观察至6 h结束时,未出现凝固。样品1、2各5个可疑菌落经血平板培养后均表现为菌落形态较大、圆形、湿润、周围可见较大透明溶血圈,与阳性标准菌株ATCC6538-1在血平板上的形态一致,阴性对照ATCC25922-1在血平板上无菌落生长,经生化鉴定,样品1、2各5个可疑菌落均为金黄色葡萄球菌,鉴定后计算结果为7 900 CFU·g-1、8 400 CFU·g-1。
2.3 3M PetrifilmTM金黄色葡萄球菌测试片结果
经培养后,测试片中出现紫红色和蓝绿色两种形态的菌落,对照3M PetrifilmTM金黄色葡萄球菌测试片说明书,紫红色的菌落是金黄色葡萄球菌,而除紫红色外的其他颜色菌落为干扰菌,排除,对两种菌落进行计数,确定10-2为最适宜计数浓度,将该浓度金黄色葡萄球菌计数结果乘以相应浓度得样品1菌落结果为8 000 CFU·g-1,样品2菌落结果为8 300 CFU·g-1,计数片结果如表2所示。
3 结论与讨论
本次能力验证,国标方法与3M PetrifilmTM金黄色葡萄球菌测试片计数法测得乳粉样品中金黄色葡萄球菌含量十分相近,进一步验证了国标方法结果的准确性,填报时以作业指导书中规定的国标方法结果为准,最终组织能力考核单位根据所有参加能力考核单位的结果计算的本次能力验证结果为满意。通过本次能力验证总结出以下注意事项。①考核样检测一定要根据作业指导书操作,尤其是样品前处理,要反复研读作业指导书中的操作步骤,再进行操作。②BP平板接种样品前,要先将平板上的水珠放在生物安全柜内出风口烘干,如果未烘干,接种平板后,平板吸收缓慢,易出现菌落连片生长现象,不易观察计数。③血浆凝固酶试验最适观察时间为每30 min观察1次,避免观察太频繁或观察时晃动力度过大,将凝固块摇碎,影响结果判断。
参考文献
[1]路桂芬,韩深.以新版《检测和校准实验室能力认可准则》(CNAS-CL01:2018)要求开展检测方法验证的问题及解决方法[J].食品安全质量检测学报,2020,11(2):638-642.
[2]韩塔拉,王俊瑞.金黄色葡萄球菌异质性耐药机制及实验室检测技术[J].中国感染控制杂志,2022,21(12):1249-1256.
[3]易小利,陈玟妃.食品中金黄色葡萄球菌检测能力验证结果分析与讨论[J].现代食品杂志,2024,30(7):168-172.
[4]中华人民共和国国家卫生健康委员会,国家市场监督管理总局.食品安全国家标准 预包装食品中致病菌限量:GB 29921—2021[S].北京:中国标准出版社,2021.
[5]中华人民共和国国家卫生健康委员会,国家市场监督管理总局.食品安全国家标准 散装即食食品中致病菌限量:GB 31607—2021[S].北京:中国标准出版社,2021.
作者简介:杨生梅(1992—),女,甘肃武威人,硕士,工程师。研究方向:食品微生物检测。
通信作者:段爱莉(1986—),女,甘肃定西人,硕士,高级工程师。研究方向:食品安全检测。E-mail: 404615320@qq.com。