超高效液相色谱-串联质谱法测定配制酒中甜蜜素的含量
作者: 刘慧 张啸怡 何青科 徐文泱
摘 要:建立配制酒中甜蜜素含量的超高效液相色谱-串联质谱测定方法,并开展方法学验证,甜蜜素在5~500 ng·mL-1线性关系良好,检出限和定量限分别为0.01 mg·kg-1和0.05 mg·kg-1。配制酒样品在
2.5 mg·kg-1、5.0 mg·kg-1、10.0 mg·kg-1加标水平下甜蜜素的加标回收率为99.0%~100.6%,相对标准偏差为0.8%~1.6%。通过测定23份配制酒样品,比较本方法和GB 5009.97—2016高效液相色谱法二者测定结果的差异。结果显示,12份样品均检出甜蜜素,两种方法结果相对偏差为-9.7%~5.7%;6份样品高效液相色谱法未检出,本方法有检出,在一定程度可避免“假阴性”结果。该方法简便、快速、准确、灵敏,可为打击配制酒中甜蜜素超量使用等违法违规行为提供检验依据,以满足食品安全监管需求。
关键词:甜蜜素;超高效液相色谱-串联质谱法;配制酒
Determination of Sodium Cyclamate in Blending Liquor by UPLC-MS/MS
LIU Hui, ZHANG Xiaoyi, HE Qingke, XU Wenyang*
(Hunan Provincial Institute of Product and Goods Quality Inspection, Hunan Provincial Key Laboratory of Food Safety Monitoring and Early Warning, Changsha 410017, China)
Abstract: A method for the determination of sodium cyclamate in blending liquor has been established and validated based on ultra-high performance liquid chromatography-tandem mass spectrometry. The result showed that the working curve of sodium cyclamate was linear in the range of 5~500 ng·mL-1. The limit of detection and limit of quantification of the method were 0.01 mg·kg-1 and 0.05 mg·kg-1, respectively. The recoveries of sodium cyclamate at the spiked levels of 2.5 mg·kg-1, 5.0 mg·kg-1, and 10.0 mg·kg-1g were 99.0%~100.6%, and the relative standard deviations were 0.8%~1.6%. Comparing the results of this method with GB 5009.97—2016 (high-performance liquid chromatography) on 23 blending liquor samples, 12 samples showed positive results by both the two methods, and the relative deviations of the two methods were -9.7%~5.7%. However, 6 samples showed the negative results by high-performance liquid chromatography, in contrast, positive results by this method, which indicates that this method can avoid “false negative” results to some extent. The method is simple, rapid, accurate, and sensitive, and it can provide a testing basis for cracking down on illegal and irregular behaviors such as the use of sodium cyclamate over legal limits in blending liquor to meet the demand of food safety supervision.
Keywords: sodium cyclamate; ultra-high performance liquid chromatography-tandem mass spectrometry; blending liquor
甜蜜素(环己基氨基磺酸钠)是一种以环己胺为原料,经氯磺酸或氨基磺酸化形成环己基氨基酸磺酸后与氢氧化钠作用而制成的人工合成甜味剂,其甜度是蔗糖的30~80倍,常在配制酒、冷冻饮品、腌渍蔬菜、饼干、饮料、糕点、蜜饯和复合调味料等食品中添加使用。人体不吸收甜蜜素,几乎全部以原型经粪便排出,在体内不
蓄积[1]。
配制酒通常以发酵酒或蒸馏酒及食用酒精为酒基,加入可食用动植物组织或既是食品又是中药材的物质,辅加食品添加剂用于呈色呈味。由于甜蜜素具有较好的改善配制酒风味和口感的作用,部分配制酒生产者在实际生产过程中通常会添加一定量的甜蜜素以调整配制酒的适口性。《食品安全国家标准 食品添加剂使用标准》(GB 2760—2014)[2]规定,配制酒中甜蜜素的最大使用量为0.65 g·kg-1(以环己基氨基磺酸计)。临床实践表明,长期或过量摄入甜蜜素,尤其是此类合成甜味剂,会对人体的代谢系统、神经系统等造成影响[3-4]。联合国粮农组织和世界卫生组织食品添加剂联合专家委员会建议其每日容许摄入量为0~11 mg·(kg bw)-1。
目前,测定食品中甜蜜素的检测方法主要包括分光光度法[5]、液相色谱法(LC)[6]、气相色谱法[7-8]、
离子色谱法[9]、气相色谱质谱联用法[10-11]和液相色谱质谱联用法[12-14]。对于配制酒中甜蜜素测定的现行有效的食品安全国家标准方法为GB 5009.97—2016第二法 高效液相色谱法[15],该方法通过衍生化将环己基氨基磺酸钠水提后,在强酸性溶液中与次氯酸钠反应,生成N,N-二氯环己胺,经正庚烷萃取,利用高效液相色谱法检测,操作烦琐,定量限为
0.030 g·kg-1,易出现“假阴性”结果。
由于超高效液相色谱-串联质谱法具有快速分离、灵敏度高、选择性高的优势,已广泛应用于白酒、饮料、糕点和面制品中甜蜜素的测定。本文以配制酒和甜蜜素为研究对象和目标,开展相关方法学考察,建立配制酒中甜蜜素的测定方法。通过实际样品测定,比较本方法和GB 5009.97—2016高效液相色谱法二者测定结果的差异,为实现开发配制酒中甜蜜素简便、快速、准确、灵敏的液质联用检测方法提供研究基础,为打击配制酒中甜蜜素超量使用等违法违规行为提供检验依据,以满足食品安全监管需求。
1 材料与方法
1.1 材料与仪器
配制酒样品23批次,来源于湖南省流通和生产领域的监督抽查;环己基氨基磺酸钠标准品,C6H11NHSO3Na,CAS:139-05-9,纯度≥99.9%,
0.25 g,DR;甲醇,色谱纯,上海安谱实验科技股份有限公司;乙酸铵,色谱纯,阿拉丁生化科技股份有限公司;超纯水采用Milli-Q制备(18.2 MΩ·cm)。
Thermoscientific Vanquish+TSQ QUANTIS超高效液相色谱质谱联用仪;Sartorius SECURA225D-1CN分析天平。
1.2 溶液的配制
(1)标准储备液。准确称取11.2 mg环己基氨基磺酸钠用水溶解定容至10 mL,摇匀,制成浓度为
1.0 mg·mL-1的标准溶液。
(2)标准中间液。吸取上述标准储备液适量,用水溶解定容至10 mL,摇匀,制成浓度为1.0 μg·mL-1的标准中间液。
(3)标准曲线系列工作液。吸取上述标准中间液适量,用水逐级稀释制成5 ng·mL-1、10 ng·mL-1、
20 ng·mL-1、50 ng·mL-1、100 ng·mL-1、200 ng·mL-1和500 ng·mL-1标准系列溶液。
1.3 样品前处理
称取样品1.0 g置于100 mL比色管中,加水稀释至刻度,摇匀,过0.22 μm滤膜,待测。
1.4 仪器条件
1.4.1 液相色谱条件
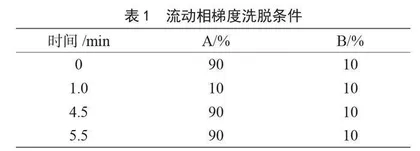
色谱柱:Hypersil GOLD C18(150 mm×2.1 mm,3 μm);柱温:30 ℃ ;进样量:5 μL;流速:
0.2 mL·min-1;流动相:10 mmol·L-1乙酸铵(A)和甲醇(B),梯度洗脱条件见表1。
1.4.2 质谱条件
扫描方式:正离子扫描(ESI-);毛细管电压:
2 500 V;鞘气流速:20 Arb;辅助气流速:5 Arb;离子传输管温度:325 ℃;离子源温度:350 ℃;扫描方式:多反应离子监测(MRM),条件见表2。
2 结果与分析
2.1 试验条件优化
2.1.1 样品前处理
配制酒的酒基为蒸馏酒及食用酒精或发酵酒,因此配制酒中含有一定浓度的乙醇。根据白酒中甜蜜素分析方法前处理过程需于60 ℃水浴加热30 min去除酒精,考虑配制酒中乙醇含量对测定结果的影响,本试验比较挥发样品中乙醇(60 ℃水浴上加热30 min)与直接用水稀释两种前处理方式对甜蜜素测定结果的影响,结果见表3。3个浓度水平两种前处理方式的测定结果相对偏差为-12.2%~5.0%,无明显差别,可能是因为配制酒不同于高乙醇含量的白酒,其乙醇浓度偏低,用水稀释后,乙醇对测定结果的影响可忽略不计。直接稀释处理进样快速、简便,因此,本试验选择直接用水稀释进样分析。
2.1.2 色谱与质谱条件
由于甜蜜素(环己基氨基磺酸钠)以钠盐形式存在,在水溶液中易电离形成[M-Na]-,适合负离子模式进行检测。ESI离子化过程主要受化合物浓度、表面活性、基质(溶剂)性质、pH值以及流速的影响,在流动相中添加适当的改性剂如甲酸、氨水、乙酸铵,有助于提高化合物离子化效率和改善峰型。负离子模式下,乙酸铵、氨水更容易夺取溶剂中的H+,从而促使甜蜜素从分子态向离子态的转化,提高电离效率。但考虑到氨水对色谱柱的损伤,本试验采用乙酸铵作为改性剂,通过比较5 mmol·L-1、10 mmol·L-1、15 mmol·L-1乙酸铵溶液对响应和峰形的影响发现,在10 mmol·L-1乙酸铵甜蜜素响应好且峰形佳,因此最终采用10 mmol·L-1乙酸铵水溶液作为流动相。
2.2 方法学验证
2.2.1 专属性
按上述过程制备配制酒样品、配制酒样品中加入标准溶液的基质加标样品,吸取空白溶剂、标准溶液、样品溶液和基质加标溶液进样分析,色谱图见图1。样品溶液与基质加标溶液色谱在甜蜜素峰位有相同的色谱峰出现,而空白溶液在相应位置上无其他干扰峰,方法专属性良好。
2.2.2 标准曲线
取1.2项下标准曲线系列工作液,按上述条件测
定,以甜蜜素峰面积为纵坐标、浓度为横坐标绘制标准
曲线,得出甜蜜素线性方程为y=7.886×103x-2.631×