荧光微球免疫层析法快速检测基围虾中环丙沙星
作者: 刘妍 李晓璐
摘 要:本研究将环丙沙星单抗与带羧基的荧光微球偶联标记,将环丙沙星抗原和羊抗鸡IgY分别包被于硝酸纤维膜上作为检测线(T)和控制线(C),然后根据其荧光信号比值(T/C)和样本中环丙沙星药物浓度之间的对应关系建立了一种简单快速、高灵敏检测基围虾样本中环丙沙星药物残留的荧光微球定量免疫层析检测方法,检测过程可在15 min内完成。结果表明,在最优条件下,基围虾样本中的环丙沙星检测范围为0~
10 ng·mL-1,检测限为0.208 ng·mL-1,回收率为90.59%~111.70%,变异系数为4.20%~10.76%。特异性实验表明环丙沙星抗体与其他喹诺酮类药物交叉反应率较低。本方法灵敏度高、准确度高、性能稳定、特异性好,可较好地满足现场快速定量检测基围虾样本中环丙沙星药物残留的需要。
关键词:环丙沙星;荧光微球;免疫层析;快速检测
Rapid Detection of Cyprofloxacin in Metapenaeus ensis by Fluorescence Microsphere Immunochromatography Method
LIU Yan, LI Xiaolu*
(Zhongshan Torch Polytechnic, Zhongshan 528436, China)
Abstract: In this study, ciprofloxacin antibody was conjugated and labeled with carboxyl fluorescent microspheres, and ciprofloxacin antigen and anti-chicken IgY were coated on nitric acid fiber membrane as detection line (T) and control line (C), respectively. Then, a fluorescence microsphere quantitative immunochromatography method with simple, rapid and highly sensitive for detection of cyprofloxacin residues in samples of Metapenaeus ensis was developed according to the corresponding relationship between the fluorescence signal ratio (T/C) and the concentration of cyprofloxacin. The whole inspection process can be completed within 15 minutes. These results showed that under optimized conditions, the detection range of ciprofloxacin was 0~10 ng·mL-1, the detection limits of ciprofloxacin in Metapenaeus ensis was 0.208 ng·mL-1 with recovery rate ranging from 90.59% to 111.70%, and the coefficient of variation ranged from 4.20% to 10.67%. In addition, the specificity test showed that ciprofloxacin antibody had low cross-reaction rate with other quinolones. The method established in this study has the characteristics of good sensitivity, high accuracy, stable performance and good specificity, which can meet the needs of rapid and quantitative detection of cyprofloxacin residues in Metapenaeus ensis samples.
Keywords: ciprofloxacin; fluorescentmicrospheres; immunochromatography; rapid detection
环丙沙星是目前使用较为广泛的第三代合成喹诺酮类抗菌药物,具有抗菌谱广、抗菌活性强、口服易吸收及价格低廉等特点,主要应用于临床实践和畜牧疾病的防治,以提高动物性食品的质量[1-2]。但是,环丙沙星会在动物体内发生转化和富集,造成一定程度的药物残留[3-4]。众多研究表明,环丙沙星在动物性食品中的药物残留可直接危害人体健康,造成环境污染,影响养殖业的健康发展[5]。随着饲养食用动物数量的大量增加,动物性食品中的环丙沙星药物残留问题已引起国际社会的广泛关注。中国、美国、日本以及欧盟均对环丙沙星在食品中的残留情况做出了严格的规定[6]。
动物食品中环丙沙星的传统检测方法主要有液相色谱法、酶联免疫法、电化学分析法及微生物分析法等,但这些方法均存在操作烦琐、设备庞大、检测时间较长等缺点,难以满足兽药残留检测方法对快速、高通、自动化的要求[7-8]。荧光免疫层析技术是基于抗原抗体特异性免疫反应的新型检测技术,具有速度快、检测成本低、灵敏度高等特点,适合大量样本的快速分析,但传统荧光免疫分析技术容易发生荧光淬灭问题,且处理数据需要专门的扫描设备,检测成本高[9]。荧光微球免疫快速检测技术将荧光素包裹在荧光微球中,巧妙避免了基质和荧光素的近距离接触,一定程度上解决了荧光信号的淬灭问题。大量荧光分子的包埋不仅增强了检测灵敏度,也提高了定量检测的效率,较好地解决了荧光免疫层析技术存在的问题[10-12]。目前,荧光微球免疫层析应用于检测食品中的喹诺酮类药物残留已有少量报道,但回收率较低(≤50%),交叉反应率较大(≥50%),灵敏度和特异性有待进一步提高[13-14]。
本研究将羧基化荧光微球用于抗体的共价偶联以提高标记物的稳定性,然后对预处理方法进行优化,建立了一种简单、快速、高灵敏的基围虾肉中环丙沙星残留的荧光定量免疫层析检测方法,并考察了环丙沙星与其他喹诺酮类药物的交叉反应率,以期为基层现场监测动物性食品中的喹诺酮类药物残留提供较好的工作基础。
1 材料与方法
1.1 材料与试剂
环丙沙星-BSA抗原、环丙沙星单抗,广州优抗多生物技术有限公司;羊抗鸡IgY抗体,杭州启泰生物技术有限公司;羧基化荧光微球,上海辉质有限公司;1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDC·HCl)、N-羟基硫代琥珀酰亚胺,阿拉丁试剂(上海)股份有限公司(上海,中国);海藻糖、葡聚糖、牛血清白蛋白,Tris及吐温,国药集团化学试剂有限公司(上海,中国);玻璃纤维素垫、吸水纸、PVC底板,通成纸制品有限公司(怀远,中国);试纸条卡壳,青岛广达森塑胶有限公司;硝酸纤维素膜,Millipore(Bedford, MA, USA);ProClin300,SUPELCO公司(Pennsylvania,美国);其他所用试剂均购自国药集团化学试剂有限公司(上海,中国),且均为分析纯。试验用活化缓冲液、偶联缓冲液、微球保存液、包被抗体稀释液、结合垫处理液、样品垫处理液、喷膜稀释液和样本稀释液等溶液均为实验室自制;实验中所用超纯水(≥18.2 MΩ)使用Millipore公司的Milli-Q system(美国)制备。
1.2 仪器与设备
真空旋转浓缩仪,德国Eppendorf公司;KQ5200超声波清洗器,昆山市超声仪器有限公司;电子防潮柜,杭州智硕电子科技有限公司;真空鼓风干燥箱,上海姚氏仪器设备厂;AFS-1000荧光免疫分析仪,广州蓝勃生物科技有限公司;均质机,广州蓝勃生物科技股份有限公司;液相色谱-质谱联用仪、喷金划膜仪、斩切机和压壳机,上海金标生物科技有限公司。
1.3 实验方法
1.3.1 荧光微球与环丙沙星单抗的偶联
取1 mg荧光微球(10 mg·mL-1),依次加入
5 μL活化缓冲液配制的EDC·HCl溶液(5 mg·mL-1)和15 μL N-羟基琥珀酰亚胺(NHS)溶液(5 mg·mL-1),室温反应30 min。4 ℃条件下13 000 r·min-1离心
35 min,去上清,再加入1 mL的超纯水,在4 ℃条件下13 000 r·min-1离心35 min,去上清,并重复1次。然后加入1 mL偶联缓冲液,按照微球与抗体10∶1的质量比加入0.1 mg环丙沙星抗体,涡旋混匀后,室温振荡反应120 min。然后加入75 mg·mL-1甘氨酸和100 mg·mL-1的BSA进行封闭,室温振荡反应过夜。4 ℃条件下13 000 r·min-1离心35 min,去上清,加入1 mL保存缓冲液,超声分散后,再加入1 mL保存缓冲液,重复2次,即可得到偶联的荧光微球-环丙沙星抗体复合物,做好标识,2~8 ℃下干燥储存备用。
1.3.2 荧光微球与羊抗鸡IgY的偶联
荧光微球偶联羊抗鸡IgY的过程参照1.3.1即可。
1.3.3 结合垫处理和样品垫处理
结合垫、样品垫分别用结合垫处理液、样品垫处理液浸泡5 min后,沥干,于42 ℃左右的干燥箱内烘干。然后取出放在密封袋内,并加适量干燥剂,密封,做好标识,放置于防潮柜中备用。保存和使用过程中应严格防潮,湿度要求≤30%。分别取预先偶联好的荧光微球-环丙沙星抗体复合物、荧光微球-羊抗鸡IgY复合物,分别稀释5倍、40倍后混合,用喷金划膜仪将混合溶液喷涂在处理后的结合垫上。喷好后,37 ℃干燥2 h。
1.3.4 环丙沙星-BSA抗原、鸡IgY划线
用包被抗体稀释液将环丙沙星-BSA抗原稀释成1 μg·mL-1作为检测线(T线),将鸡IgY稀释成
0.1 mg·mL-1作为质控线(C线)。用喷金划膜仪将上述两种溶液包被在NC膜上,包被完后,于37 ℃干燥2 h。
1.3.5 荧光微球免疫层析试纸条的组装
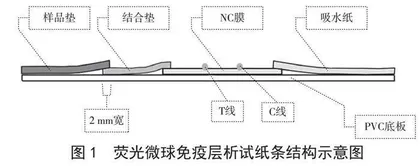
荧光微球免疫层析试纸条结构如图1所示。将处理过的样品垫、喷有微球-抗体复合物的结合垫、包被有T、C线的NC膜和吸水纸依次粘贴在PVC背板上,然后用微电脑自动斩切机切成宽度为4.0 mm的试纸条,组装塑料卡壳后,用铝箔袋封装保存备用。
图1 荧光微球免疫层析试纸条结构示意图
1.3.6 实验条件的优化
(1)荧光微球与环丙沙星单抗偶联量的优化。分别向1 mg微球中加入0.02 mg、0.05 mg、0.10 mg和0.20 mg环丙沙星单抗,制备不同偶联比例的微球-抗体复合物,相同条件下组装成试剂条进行检测,观察检测限、信噪比等。
(2)荧光微球与环丙沙星单抗偶联封闭条件的优化。单独使用75 mg·mL-1甘氨酸(Glycine,GLY)、100 mg·mL-1牛血清蛋白(Bovine albumin,BSA),以及同时使用75 mg·mL-1甘氨酸和100 mg·mL-1 BSA,分别对荧光微球与环丙沙星单抗偶联进行封闭,观察检测限、重复性等。
(3)环丙沙星-BSA单抗包被浓度的优化。用包被抗体稀释液将环丙沙星-BSA抗原稀释到浓度分别为0.1 μg·mL-1、0.5 μg·mL-1、1.0 μg·mL-1和2.0 μg·mL-1,并分别包被到NC膜上制备试纸条进行检测,每个试验测试3次,观察检测限、线性关系等。
(4)环丙沙星类药物的检测。用样本稀释液稀释环丙沙星制备梯度检测试样,取待测溶液100 μL,
从层析试纸条的样品滴加处开始滴加。等待10 min,再用荧光测试仪检测含待测溶液的试纸条。待测样本中不含环丙沙星时,检测区(T)与质控区(C)均出现亮线。待测样本中环丙沙星含量增加,检测区亮线则逐渐减弱,直至消失,而质控区始终保持亮线。因此,根据检测区荧光峰强度(T)和质控区荧光峰强度(C)的比值,即T/C值来实现对环丙沙星的检测。