加味归芪片质量标准研究
作者: 王娟弟 李敏 刘蕊 郭晓霞 李欣 李冬华 马潇 郭朝晖
摘要 [目的]提高加味归芪片的质量标准。[方法]采用色谱柱Agilent Eclipse Plus C18(4.6 mm×250 mm,5 μm),以乙腈-0.085%磷酸溶液(17∶83)为流动相,检测波长为316 nm,柱温35 ℃,测定阿魏酸的含量;采用蒸发光散射检测器测定黄芪甲苷的含量,以Agilent Eclipse Plus C18(4.6 mm×250 mm,5 μm)为色谱柱,乙腈-水(32∶68)为流动相;采用薄层色谱法分别对处方中的当归和黄芪进行定性鉴别。[结果]阿魏酸在2.265~22.651 μg/mL呈良好的线性关系(R2=0.999 9),平均回收率为97.38%,相对标准偏差(RSD)为1.93%,每片含量在29.6~34.0 μg;黄芪甲苷在70.65~495.55 μg/mL呈良好的线性关系(R2=0.999 8),平均回收率为93.92%,RSD为2.59%,每片含量在0.383~0.449 mg;当归和黄芪薄层色谱斑点清晰,阴性对照无干扰。[结论]该方法简单、准确、可靠,可行性和重复性良好,能有效控制加味归芪片的质量。
关键词 加味归芪片;质量标准;薄层色谱法;高效液相色谱法
中图分类号 R286.0 文献标识码 A 文章编号 0517-6611(2023)19-0147-06
doi:10.3969/j.issn.0517-6611.2023.19.034
Study on Quality Standard of Jiawei Guiqi Tablet
WANG Juan-di1,2, LI Min1,2, LIU Rui1,2 et al
(1.Gansu Provincial Institute of Drug Control, Lanzhou, Gansu 730070; 2.NMPA Key Laboratory for Quality Control of TCM, Lanzhou, Gansu 730070)
Abstract [Objective]To improve the quality standard of Jiawei Guiqi tablets.[Method]The Agilent Eclipse Plus C18 (4.6 mm×250 mm,5 μm) column was used with acetonitrile -0.085% phosphoric acid (17∶83) as mobile phase.The detection wavelength was 316 nm and the column temperature was 35 ℃.The content of ferulic acid in Jiawei Guiqi tablet was determined.The HPLC method with Evaporative Light Scattering Detector (ELSD) was established to determine the content of Astragaloside IV in in Jiawei Guiqi tablet.Using Agilent Eclipse Plus C18 (4.6 mm×250 mm,5 μm) column.Acetonitrile-water (32∶68) as mobile phase.TLC was used to identify Chinese angelica and radix astragali.[Result]The linear range of ferulic acid was 2.265-22.651 μg/mL (R2=0.999 9).The average recovery was 97.38%, the relative standard deviation (RSD) was 1.93%,the content of ferulic acid in Jiawei Guiqi tablet ranged from 29.6 to 34.0 μg.The linear range of Astragaloside IV was 70.65-495.55 μg/mL (R2=0.999 9).The average recovery was 93.92%, the relative standard deviation (RSD) was 2.59%.The content of astragaloside IV in each tablet ranged from 0.383 to 0.449 mg.TLC spots of chinese angelica and radix astragali were clear, and negative control had no interference.[Conclusion]This method is simple ,accurate,reliable,feasible and repeatable,can be used to effectively control the quality of Jiawei Guiqi tablets.
Key words Jiawei Guiqi tablet;Quality standard;TLC;HPLC
加味归芪片收载于1992年出版的卫生部药品标准《中药成方制剂》第六册(WS3-B-1118-92),具有补气、养血之功效,用于气血两亏、气虚体弱、肢体劳倦之症[1],该制剂疗效明确、适用人群广、副作用小;其处方中的3味药材当归、黄芪、党参均属于甘肃省道地药材。
当归是伞形科植物当归[Angelica sinensis(Oliv.)Diels]的干燥根,具有补血活血等功效,主要分布在甘肃、四川及云南等地,甘肃岷县被誉为“千年药乡”,其产当归品质优良,又被称为岷归;其主要含有挥发油、有机酸、多糖和黄酮等成分[2-8]。2020年版《中国药典》[9]以阿魏酸作为评价当归药材和饮片质量的指标性成分之一。
黄芪是豆科植物蒙古黄芪[Astragalus membranaceus Bge.var.mongholicus(Bge.) Hsiao]和膜荚黄芪[A.membranaceus(Fisch.) Bge.]的根,具有补气固表、利尿脱毒、排脓、敛疮生肌的功效,主要分布在甘肃、内蒙古和山西等地;其主要含有多糖类、皂苷类、黄酮类、生物碱类等成分[10-15]。2020年版《中国药典》[9]以黄芪甲苷作为评价黄芪药材和饮片质量的指标性成分之一。
加味归芪片质量标准的内容简单,仅有性状、显微鉴别、片剂通则项,不能有效控制产品质量。为此,该研究拟对加味归芪片质量标准进行提升,提高产品质量,从而更加有效控制加味归芪片的质量,确保加味归芪片的疗效,为临床用药提供质量保证。
1 仪器与材料
1.1 仪器
高效液相色谱仪(日立,型号Chromaste);电子天平(瑞士梅特勒公司,型号ME204、MS205DU);旋转蒸发仪(瑞士BUCHI公司,型号Rotavapor R-300);离心机(艾本德公司,型号5810R);薄层色谱点样仪(瑞士卡玛公司,型号ATS4)。
1.2 试药与样品
当归(中国食品药品检定研究院,批号120927-201617);阿魏酸(中国食品药品检定研究院,批号110773-201614);黄芪甲苷(中国食品药品检定研究院,批号120974-21813);甲醇、乙腈均为色谱级;水为屈臣氏水;其余试剂均为分析纯。加味归芪片(批号180501、181101、190101、190701、191201、191202、191203、191204、200101、200102、200103、200104)来源于佛仁制药有限公司。
2 方法与结果
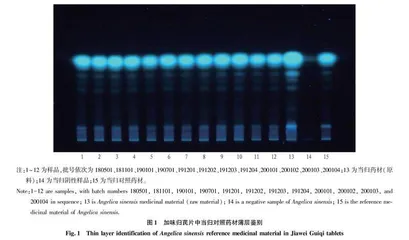
2.1 当归成分的薄层色谱鉴别 取本品适量,去包衣,粉碎,精密称定粉末5 g,加乙醚20 mL,超声处理10 min,滤过,滤液蒸干,残渣加乙醇1 mL溶解,作为供试品溶液。另取当归阴性药材5 g、当归药材(原料)0.5 g、当归对照药材0.5 g,同法制成当归阴性对照溶液、当归药材(原料)和当归对照药材溶液。按照薄层色谱法(通则0502)试验,吸取上述3种溶液各10 μL,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯(4∶1)为展开剂,展开,取出,晾干。置紫外光灯(365 nm)下检视,结果见图1。
取本品适量,去包衣,粉碎,精密称定粉末5 g,加1%碳酸氢钠溶液50 mL,超声处理10 min,6 000 r/min离心5 min,取上清液用稀盐酸调节pH至2~3;用乙醚振摇提取2次,每次20 mL,合并乙醚液,挥干,残渣加甲醇1 mL溶解,摇匀,作为供试品溶液。另取当归阴性药材5 g、当归药材(原料)0.5 g,同法制成当归阴性和当归药材(原料)对照溶液。另取阿魏酸对照品,加甲醇制成1 mg/mL溶液,作为对照品溶液。按照薄层色谱法(通则0502)试验,吸取上述3种溶液各10 μL,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯-二氯甲烷-甲酸(4∶1∶1∶0.1)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视,结果见图2。
加味归芪片样品、当归对照药材以及阿魏酸对照品均有相应的斑点,斑点清晰,分离条件好,并且加味归芪片当归阴性无干扰,因此对当归对照药材和阿魏酸对照品进行定性鉴别。
2.2 黄芪成分的薄层色谱鉴别 取本品适量,去包衣,粉碎,精密称定粉末5 g,置锥形瓶中,加甲醇30 mL,超声处理30 min,放冷,过滤,收集滤液,蒸干,残渣溶解于10 mL 10%(V/V)氨水溶液中,待溶解完全,将溶液转移至分液漏斗中,用水饱和的正丁醇萃取3次(15、10、10 mL)。合并提取液,蒸干,残渣用甲醇溶解并转移至10 mL容量瓶中,加甲醇至刻度,即得。取黄芪对照药材1 g、黄芪药材(原料)1 g、黄芪阴性样品5 g,同法制备对照药材和黄芪药材(原料)溶液及阴性对照溶液。取黄芪甲苷对照品,加甲醇制成1 mg/mL溶液,即得对照品溶液。按照薄层色谱法(通则0502)试验,吸取上述溶液5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(2∶4∶2∶1)的下层溶液作为展开剂,取出,晾干,喷以10%硫酸乙醇,105 ℃干燥之显色,置紫外光(365 nm)下检视,结果见图3。
加味归芪片样品与黄芪甲苷对照品有相应的斑点,斑点清晰,分离条件好,且黄芪阴性无干扰。加味归芪片样品与黄芪对照药材有相应的斑点,斑点清晰,但黄芪阴性有干扰。因此对黄芪甲苷对照品进行定性鉴别。
2.3 阿魏酸含量测定
2.3.1 色谱条件。色谱柱为Agilent Eclipse Plus C18(4.6 mm×250 mm,5 μm);以乙腈-0.085%磷酸溶液(17∶83)为流动相;检测波长为316 nm;柱温35 ℃。
2.3.2 对照品溶液的制备。取阿魏酸对照品11.44 mg,精密称定,置50 mL棕色量瓶中,加70%甲醇制成0.228 8 mg/mL的溶液,作为储备液。
2.3.3 供试品溶液的制备。取本品20片,除去包衣,研细(过三号筛),取约2 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇25 mL,密塞,称定重量,加热回流1 h,放冷,再称定重量,用70%甲醇补足减失的重量,摇匀,静置,取上清液滤过,取续滤液,即得。