营养风险筛查的标准营养支持治疗对胃癌术后患者PA及CD4/CD8表达水平的影响
作者: 陈晓燕 俞远怀
摘要:目的:分析营养风险筛查的标准营养支持治疗对胃癌术后患者PA及CD4/CD8表达水平的影响。方法:选取2020年1月—2022年12月我院住院治疗的胃癌术后90例作为研究对象,均有手术史,根据术后营养管理方式不同分为研究组和对照组,每组各45例。对照组采用常规营养支持,研究组给予营养风险筛查的标准营养支持治疗。比较两组的营养状况、并发症。结果:治疗前两组患者的营养指标、T淋巴细胞亚群水平均无明显差异(P>0.05)。治疗后研究组的血清白蛋白(ALB)、前白蛋白(PA)、转铁蛋白(TRF)水平以及CD3+、CD4+、CD4+/CD8+水平均高于对照组,研究组的胃肠功能恢复时间、正常饮食时间、住院时间均短于对照组,术后并发症总发生率低于对照组,有统计学意义(P<0.05)。结论:营养风险筛查的标准营养支持治疗可提高胃癌术后患者PA及CD4/CD8表达水平,改善营养状况,促进机体恢复,同时减少并发症。
关键词:营养风险筛查;标准营养支持;胃癌术后;营养状况
现阶段胃癌的临床治疗是以手术治疗为主的系统化综合治疗方法[1-4],胃癌术后患者可出现多种并发症,由于胃肠道症状显著,可对其进食产生严重影响,因此营养不良是最常见的并发症,不利于术后并发症的防治和恢复[5]。胃癌术后营养支持是改善营养状况的重要手段,可促进疾病的恢复,减少术后并发症对机体的影响[6-7]。基于此,本研究主要分析营养风险筛查的标准营养支持治疗对胃癌术后患者PA及CD4/CD8表达水平的影响。
1 对象和方法
1.1 对象
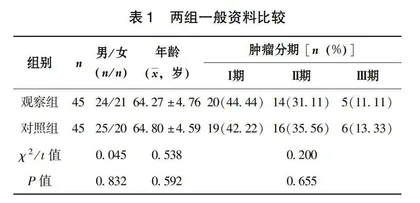
选取2020年1月—2022年12月,于我院住院治疗的胃癌术后90例作为研究对象,根据术后营养管理方式不同分为研究组和对照组,每组各45例。两组患者的一般资料比较,未见统计学差异(P>0.05)(表1)。本研究经院内医学伦理委员会审核批准。纳入标准:①符合胃癌筛查诊断标准[8];②符合术后营养支持治疗指征;③患者及家属知情同意。排除标准:①伴有其他恶性肿瘤;②伴有其他非肿瘤类严重疾病,如感染、免疫系统疾病、血液系统疾病等;③伴有机体重要脏器功能障碍疾病者;④合并认知功能障碍、精神疾病或精神病史。
1.2 方法
对照组采用常规营养支持,包括入院时正确评估患者的营养状态,根据评估结果实施相应的营养支持方案;放置胃管;术后深静脉置管,使用肠外营养液补充10~25 kcal/(kg·d)能量,患者胃肠功能恢复后拔除胃管,给予流质至正常饮食的营养管理。
研究组给予营养风险筛查的标准营养支持治疗:(1)入院时营养风险筛查,患者入院后24h内,检测血清血红蛋白、白蛋白、前白蛋白等营养指标。初级筛查:问卷调查,包括疾病严重程度、目前体重指数、近期进食量、近期体质量下降以及其他营养不良风险,如有1项存在问题即进入终筛。利用营养风险筛查2002(NRS-2002)对其营养风险情况进行评估,包括年龄、疾病严重程度、营养状态等3个方面,分别为3分、3分、1分,3~4分为低风险,5~7分为高风险。(2)标准营养支持:①针对低风险:入院后1 d给予25 g中长链脂肪乳、50 g氨基酸、100 g葡萄糖、电解质、微量元素,进行营养补充。之后使用氨基酸、脂肪乳、葡萄糖商品化三腔袋进行营养补充[30 kcal/(kg·d)]。②针对高风险:入院第1 d给予50 g氨基酸、100 g葡萄糖、25 g中长链脂肪乳、电解质、微量元素,进行营养补充。入院后第2 d给予200 mL专业肠内营养乳剂(20 mL/h)。之后第3d给予肠内营养乳剂200 mL+肠内营养混悬液500 mL(50 mL/h)。之后4~7 d,给予1 500 mL肠内营养混悬液(100 mL/d)。营养支持治疗7 d,所有患者在胃肠功能恢复营养状态后拔除胃管,24 h内给予流质饮食,24~48 h给予半流质,观察患者的情况,如恢复良好可正常饮食。
1.3 观察指标
1.3.1 营养指标 接受营养支持治疗前后均取两组患者清晨空腹静脉血5mL,使用血常规分析仪检测血清营养成分含量,包括血清白蛋白(ALB)、前白蛋白(PA)、转铁蛋白(TRF)。
1.3.2 免疫功能指标 治疗前后检测两组患者的T淋巴细胞亚群水平,包括CD3+、CD4+、CD4+/CD8+水平。
1.3.3 机体功能恢复指标 记录两组患者入院后胃肠功能恢复时间、恢复正常饮食时间、住院时间。
1.3.4 并发症发生情况 记录两组患者术后并发症情况,包括营养不良、便秘、腹痛、切口感染等。
1.4 统计学分析
采用SPSS 22.0软件对数据进行统计分析。计量资料以均数±标准差(x±s)表示,组间比较采用t检验;计数资料以n(%)表示,组间比较采用χ2检验。以P<0.05表示差异有统计学意义。
2 结果与分析
2.1 两组治疗前后营养指标比较
治疗前两组患者的营养指标无明显差异(P>0.05)。治疗后研究组的ALB、PA、TRF水平均高于对照组,有统计学意义(P<0.05)(表2)。
2.2 两组治疗前后免疫功能指标比较
治疗前两组T淋巴细胞亚群水平无明显差异(P>0.05)。治疗后研究组CD3+、CD4+、CD4+/CD8+水平均高于对照组,有统计学意义(P<0.05)(表3)。
2.3 两组机体功能恢复指标比较
研究组的胃肠功能恢复时间、正常饮食时间、住院时间均短于对照组,有统计学意义(P<0.05)(表4)。
2.4 两组术后并发症发生率比较
研究组术后并发症总发生率低于对照组,有统计学意义(P<0.05)(表5)。
3 讨论
营养是机体细胞活动的重要能量,机体营养不良状态不利于术后恢复,可导致创口愈合延迟。同时营养缺乏可引起机体免疫力降低,更容易导致感染、腹腔脓肿等并发症的发生。营养不良可对胃癌患者的预后产生直接影响,加强营养风险筛查及营养支持治疗可改善预后[9-12]。有研究表明,消化系统肿瘤患者具有较高的营养不良风险[13]。而胃癌患者的营养风险的影响因素较多,如患者自身的疾病严重情况、年龄、文化程度、家庭收入以及围手术期有无营养支持等。术前营养风险筛查对胃癌患者术后营养不良的预防具有重要作用,可改善预后[14]。但是,在以往的临床中多以医生的经验对患者的营养风险进行评估,缺乏完整的理论支撑。研究表明,NRS-2002评分是营养风险的有效评估工具,其可行性较高、可重复性好,可能科学、准确反映患者的营养状况以及疾病严重程度[15]。同时胃癌患者的营养支持也具有重要作用,标准营养支持可提高营养治疗的效果,是不可缺少的部分[16-17]。因此营养风险筛查的标准营养支持治疗是一种通过具有理论支持的营养风险筛查方式,对患者的营养状态进行全面了解、预测是否存在风险,根据结果制定具有科学依据的营养支持治疗方案[18]。李颖颖[19]研究提出,给予胃癌手术患者营养风险筛查的标准营养支持治疗可帮助改善营养状态,减少并发症,缩短住院时间。在李益萍[20]的研究中提出,使用术后早期营养标准化流程管理有利于老年胃癌患者快速康复,有效降低术后并发症情况。本研究主要是通过组间对比分析营养风险筛查的标准营养支持治疗对胃癌术后患者PA及CD4/CD8表达水平的影响,结果显示,在营养指标、T淋巴细胞亚群水平、机体功能恢复指标以及并发症方面,研究组均优于对照组(P<0.05)。证实营养风险筛查的标准营养支持治疗对PA及CD4/CD8表达水平具有积极作用,可改善营养状态,提高机体免疫力。ALB、PA、TRF水平均为机体营养物质,是临床上营养检测的重要指标。PA主要是由肝细胞合成,显示于白蛋白前方,在体内的半衰期较短,其敏感性高于ALB、TRF,一般来说病情越严重,PA水平越低。CD4/CD8比值是免疫力判断的重要指标,通常<1.4多见于恶性肿瘤疾病,其正常值在1.4~2.0之间。营养风险筛查的标准营养支持治疗是通过科学的评估指标将患者分为高风险和低风险,从而采取具有个体化的营养支持方案,具有更强的针对性,因此在研究中可明显改善营养状态,加快创口愈合,提高免疫力,减少并发症。
综上所述,营养风险筛查的标准营养支持治疗可明显提高胃癌术后患者的营养指标与免疫力指标,减少并发症,促进术后恢复,具有应用价值。
参考文献
[1]张莹,陈丽娟,白海燕.术前营养风险筛查对胃癌患者术后并发症、生活质量及预后的影响研究[J].临床和实验医学杂志,2021,20(10):1094-1097.
[2]Mariana Moreira Claudino,Jessica Rodrigues Lopes,Viviane Dias Rodrigues,et al. Postoperative complication rate and survival of patients with gastric cancer undergoing immunonutrition: A retrospective study[J]. Nutrition, 2020; 70:110590.
[3]黄凌莉. NRS2002营养风险筛查在初诊胃癌患者中的应用[J]. 中国当代医药,2021,28(17):4-7.
[4]Raghuraman Hemamalini,Kavyashree M,Balakrishnan Gurushankari, et al. Comparison of Nutrition Risk Screening 2002 and Subjective Global Assessment for predicting postoperative complications among patients undergoing elective abdominal surgery[J]. International Journal of Advanced Medical and Health Research, 2022, 9(2) : 94-100.
[5]柯清仙,颜优贞,王益,等. 基于营养风险筛查的营养支持对胃癌病人术后细胞免疫水平的影响[J]. 全科护理,2020,18(20):2522-2524.
[6]JIANG Xiao Han ,CHEN Xi Jie,CHEN Shi,et al. Compliance with Oral Nutritional Supplementation among Gastric Cancer Patients at Nutritional Risk: A Cross-Sectional Study[J]. Nutrition and Cancer, 2022, 74(9) : 10-11.
[7]倪珊珊,苏小军,李清明,等. 112例胃癌患者营养风险筛查分析[J]. 中国公共卫生,2018,34(5):767-770.
[8]赫捷,陈万青,李兆申,等.中国胃癌筛查与早诊早治指南 [J].中国肿瘤,2022,31(7):488-527.
[9]刘艳红. 基于营养风险筛查下营养支持对胃癌根治术患者的预后效果[J]. 国际医药卫生导报,2019,25(21):3647-3649.