乳粉中单核细胞增生李斯特氏菌能力验证结果及关键环节分析
作者: 蒋佳希 黄志深 王亚琦 尹玮璐 梁美丹Ability Validation Results and Key Link Analysis of Listeria monocytogenes in Milk Powder
JIANGJiaxi,HUANGZhishen,WANGYaqiYINWeilu,LIANGeidan (Guangzhou Food Inspection Institute, Guangzhou 5114oo, China)
Abstract: The laboratory participated in the Listeria monocytogenes detection ability verification project led by the National Institutes for Food and Drug Control.It was implemented inaccordance with GB 4789.30—2016and verified by real-time fluorescence PCR.The results showed that Listeria monocytogenes was not detected in sample FC0220092,and Listeria monocytogenes was detected in sample FC0222010.The testresults wereconsistent with the results published by the National Institutes for Food and Drug Control,and satisfactory results were obtained.
Keywords: milk powder; Listeria monocytogenes; ability verification; key link analysis
单核细胞增生李斯特氏菌(Listeriamonocytogenes,LM),简称单增李斯特氏菌,是一种高致病性食源性人畜共患病原体,因其极端环境适应性与临床危害性已成为全球公共卫生安全的重要挑战。该菌能在 -1.5~42∘C 生存,并且能在 4‰ 条件下仍保持繁殖能力。人类食用被单增李斯特氏菌污染的食物后,可能会引起肠胃病、脑膜炎、败血症、孕妇流产等疾病,感染后的病死率为 30%~70% ,婴幼儿、孕妇、老年人等免疫力低下人群更容易感染该菌[1-3]。该菌在自然界中广泛存在,主要污染鱼、肉、蛋、奶以及海产品及制品、蔬菜沙拉、冷冻食品等,给食品安全带来很大风险[4-5]。我国2020—2022年国家食品安全风险监测数据显示,生鲜畜禽制品中单增李斯特氏菌阳性率高达 1.7%~3.4% ,显著高于欧盟同期水平( 0.8%~ 1.2% ),引起国家和相关部门的广泛关注。因此,确保食品中单增李斯特氏菌检验结果的准确率,是食品检测机构能力建设的关键任务。
能力验证是评定和监督实验室和检验机构技术能力的重要方式之一,对实验室和检验机构是一种有效的外部质量保证活动,也是内部质量控制技术的补充[。通过能力验证,能够更加有效地评价实验室的检测能力,不断改进和提升实验室的能力水平。本实验室承担广州市监督抽检餐饮、流通、生产环节各类食品的检测任务,为了考核实验室单增李斯特氏菌检测能力,积极参与中国食品药品检定研究院举办的能力验证活动。
1材料与方法
1.1材料与试剂
样品由中国食品药品检定研究院提供,编号分别为FC02220092和FC02220010,样品为白色球状、真空包装于西林瓶,对应基质为2袋奶粉,每份 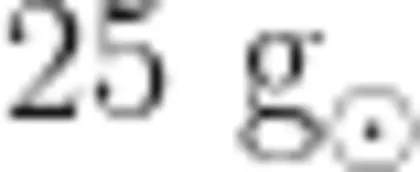
单增李斯特氏菌(ATCC19115)、英诺克李斯特氏菌(ATCC33090)、斯氏李斯特氏菌(CICC21671)以及伊氏李斯特氏菌(CICC21663)、马红球菌(ATCC6939)与金黄色葡萄球菌(ATCC25923),标准菌株均来自国家食品安全菌种保藏中心。
李氏增菌肉汤基础及配套试剂、革兰氏染色液、血平板、单增李斯特氏菌生化鉴定试剂,广东环凯微生物科技有限公司;李斯特菌显色培养基,法国科马嘉公司;PALCAM琼脂基础及配套添加剂,以及 0.6% 酵母膏的胰酪肺大豆琼脂,北京陆桥公司;VITEK2鉴定卡,法国梅里埃公司;细菌基因组DNA提取试剂盒;天根生化科技公司; 2× TaqMan qPCR MasterMix,上海东洋纺公司;引物探针,北京六合一华大基因生物公司。
1.2仪器与设备
高压灭菌锅,厦门致微公司;生化培养箱,德国宾得公司;VITEK2COMPACT全自动微生物鉴定仪器,法国梅里埃公司;生物显微镜,德国徕卡公司;ⅡI级A2型1376生物安全柜、NANODROPONE超微量分光光度计,美国ThermoFisherScience公司;96CFXtouch实时荧光PCR仪,美国Bio-Rad公司。
1.3 实验方法
1.3.1 样品的处理
按照作业指导书的要求,对样品进行如下处理在生物安全柜中,将 225mLLB1 增菌液倒入无菌均质袋,采用无菌操作打开西林瓶,将小球加入 LB1 增菌液中,待小球完全溶解后,将与西林瓶编码一致的奶粉基质样品加入 LB1 增菌液中,进行充分均质,确保样品均匀,该样品对应的待检量为 25g 。阳性对照增菌液通过将标准菌株单增李斯特氏菌(ATCC19115)加入 LB1 增菌液中制备,阴性对照增菌液则是将标准菌株英诺克李斯特氏菌(ATCC33090)加入LB1 中制备。空白对照增菌液不加入任何试剂和菌株。
本文为全文原貌 未安装PDF浏览器用户请先下载安装
原版页码:spaq20250629.pd原版全文
1.3.2 增菌与分离
参照《食品安全国家标准食品微生物学检验单核细胞增生李斯特氏菌检验》(GB4789.30—2016)[7开展前增菌,取培养 24h 后的 LB1 增菌液0.1mL 转种于 10mLLB2 增菌液内,然后用接种环取培养后 LB2 增菌液划线于李斯特显色平板和PALCAM琼脂平板, LB1 和 LB2 增菌液于 ( 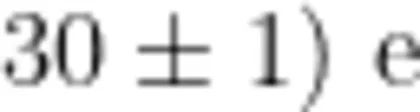 培养 24h ,李斯特显色平板和PALCAM琼脂平板于( 36±1 ) °C 培养 48h 。
培养 24h ,李斯特显色平板和PALCAM琼脂平板于( 36±1 ) °C 培养 48h 。
1.3.3 生化鉴定
挑取李斯特氏菌显色平板和PALCAM平板的可疑菌落进行纯化培养,并开展木糖和鼠李糖的初步生化试验,对木糖检测结果为阴性、鼠李糖检测检测结果阳性的菌落,再利用VITEK2compact系统开展生化鉴定、染色镜检、溶血及协同溶血试验、动力试验。
1.3.4实时荧光PCR检测
取 LB1 培养液 2mL 于 2.0mL 无菌离心管中,离心去除培养基,依照细菌DNA快速提取试剂盒操作DNA提取,并利用超微量紫外分光光度计对核酸进行浓度和质量测定,确保基因组DNA的 OD260/ OD280 均在 1.7~2.0 , -20∘C 保存备用。
参考《出口食品中食源性致病菌检测方法实时荧光PCR法》(SN/T1870—2016)[单增李斯特氏菌的引物探针序列,正向引物序列为5’-ATACGATAACATCCACGGCTCTGGCTGG-3’,反向引物序列为 5∘ -CTGAATCTCAAGCAAAACCTGGT-3’探针序列为5’-CGCGACCGAAGCCAACTA-3’其中探针的 5∘ 端标记FAM, 3⋅ 端标记TAMRA。
采用实时荧光PCR对单增李斯特氏菌进行检测,反应体系 25μL :预混液 12.5μL ,正反向引物1μL ,探针( 10μmol⋅L-1 ) 1μL ,模板DNA 2μL ,补水至 25μL 。反应条件: 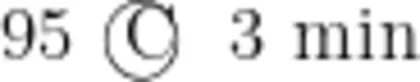 ,1个循环;
,1个循环;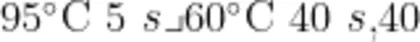 个循环,收集荧光信号。同时,实验采用阴性对照、阳性对照、空白对照进行质量控制,每个反应重复2次。
个循环,收集荧光信号。同时,实验采用阴性对照、阳性对照、空白对照进行质量控制,每个反应重复2次。
2 结果与分析
2.1增菌培养和平板分离结果
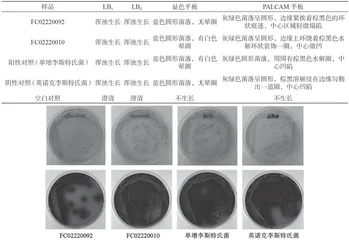
LB2 增菌液划线接种于李斯特氏菌属显色平板和PALCAM平板上的菌落形态特征见表1和图1,样品FC02220092在显示平板上为蓝色圆形菌落、无晕圈,在PALCAM平板为灰绿色圆形菌落;而样品FC02220010在显示平板为蓝色圆形菌落、有白色晕圈,在PALCAM平板为灰绿色圆形菌落,初步判定样品FC02220010可能含有单增李斯特氏菌,但为了防止漏检,对两个编号的样品均开展生化鉴定。
2.2生化鉴定结果分析
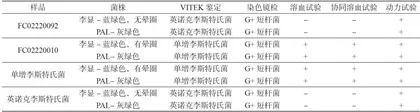
从样品FC02220092、FC02220010的显示平板和PALCAM平板中分别挑选5个典型或可疑菌落于TSA-YE平板中进行纯化培养,然后开展木糖、鼠李糖初步生化鉴定,结果符合开展VITEK生化鉴定、溶血实验、动力试验以及镜检,结果见表2。综合VITEK鉴定、革兰氏染色结果、溶血和协同溶血试验、动力试验结果,样品FC02220092未检出单增李斯特氏菌,而样品FC02220010检出单增李斯特氏菌,阴阳性对照生化鉴定结果符合质量控制的要求。
2.3实时荧光PCR检测结果
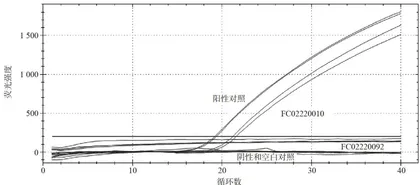
对样品FC02220092、FC02220010、阴阳性对照、空白对照的 LB1 增菌液进行DNA提取,然后按照1.3.4的体系和条件开展实时荧光PCR扩增,检测结果见图2。样品FC02220010有明显的S型扩增曲线,而FC02220092未获得S型扩增曲线,阴性对照、阳性对照、空白对照结果符合质量控制要求,说明样品FC02220092未检出单增李斯特氏菌,而样品FC02220010检出单增李斯特氏菌。
注: + 表示阳性,-表示阴性。
本文为全文原貌 未安装PDF浏览器用户请先下载安装
原版页码:spaq20250629.pd原版全文